Faktorer som har sammenheng med fatigue etter hjerneslag
Bakgrunn: Fatigue er et fremtredende symptom som ofte rammer hjerneslagpasienter. Fatigue karakteriseres som vedvarende tretthet, utmattelse og redusert energikapasitet og assosieres ofte med nedsatt livskvalitet. Tidligere studier viser stor variasjon i assosierte faktorer og forekomsten av fatigue etter hjerneslag (PSF, post-stroke fatigue).
Hensikt: Å undersøke om det er sammenheng mellom fatigue etter hjerneslag og sosiodemografiske, medisinske og kliniske karakteristika i et norsk utvalg.
Metode: Tverrsnittsstudie som inkluderte 321 hjerneslagpasienter rekruttert fra 11 sykehus i Norge i perioden 2014–2016. Vi foretok datainnsamling med strukturert spørreskjema i individuelle intervjuer 4–6 uker etter hjerneslaget. Fatigue ble målt med en kortversjon av Fatigue Questionnaire (FQ). Vi benyttet multivariat logistisk regresjonsanalyse i denne studien.
Resultat: Prevalensen av fatigue etter hjerneslag var 43,6 prosent i denne studien. Tidligere sykdommer (OR, odds ratio = 4,99), depresjon (OR = 4,47), omsorgsansvar for andre (OR = 2,86) og hjerneslagets alvorlighetsgrad (OR = 1,16) var faktorer som økte oddsen for å oppleve fatigue 4–6 uker etter hjerneslag.
Konklusjon: Studien støtter tidligere funn om at fatigue er utbredt etter hjerneslag. Studien identifiserte fire faktorer som økte oddsen for å rapportere om fatigue 4–6 uker etter hjerneslaget. Forekomsten av PSF og hvilke faktorer som er assosiert med PSF, er viktig kunnskap for sykepleiere og annet helsepersonell for å identifisere hvem som kan trenge oppfølging knyttet til fatigue etter hjerneslag.
Referer til artikkelen
Linnerud S, Bragstad L. Faktorer som har sammenheng med fatigue etter hjerneslag. Sykepleien Forskning. 2019; 14(76701):e-76701. DOI: 10.4220/Sykepleienf.2019.76701
Hvert år rammes cirka 15 000 personer av hjerneslag i Norge (1). Fatigue forekommer ofte som en subjektivt opplevd tilstand etter hjerneslag ledsaget av sterkt redusert energikapasitet, kalt post-stroke fatigue (PSF) (2, 3). I den norske befolkningen opplever rundt 10 prosent utmattelse eller fatigue (4), men forekomsten av fatigue etter hjerneslag er høyere (3).
Hjerneslag er den hyppigste årsaken til funksjonsnedsettelse hos eldre, men adekvat og tidlig rehabilitering styrker mulighetene til å gjenvinne funksjoner i dagliglivet (1). Mange pasienter opplever stor fremgang ved målrettet rehabilitering, men studier viser at PSF kan vedvare i flere år (5, 6). Studier har også vist at PSF kan oppstå på ulike tidspunkter i forløpet etter et hjerneslag (7).
PSF assosieres med nedsatt livskvalitet, redusert grad av opplevd mestring (8), redusert mulighet til å utføre daglige gjøremål (9) samt tap av kontroll i livet (10).
Hva er fatigue?
Schillinger og Becker (3) foreslår at fatigue kan defineres som «en subjektiv opplevelse av langvarig eller stadig tilbakevendende tretthet og redusert kapasitet for mental og/eller fysisk aktivitet». PSF er en tilstand som kjennetegnes av utmattelse og en utstrakt energitomhet som ofte opptrer uten forutgående fysisk eller mental anstrengelse (3).
Årsaken til PSF er ukjent, men PSF har trolig en sammensatt årsaksforklaring (11). Hvilke medisinske og sosiodemografiske faktorer som er assosiert med PSF, er uklart ettersom tidligere studier preges av motstridende funn (3, 8, 12, 13). PSF assosieres imidlertid ofte med smerter og søvnforstyrrelser (8) og er sterkt assosiert med depresjon (8, 9, 14) og angst (8, 10, 14).
Det er usikkert om sosiodemografiske faktorer som alder, kjønn, sivilstand, bosituasjon (bor alene eller ikke), utdanning og gjenopptakelse av lønnet arbeid er assosiert med PSF (3, 8). Funn fra tidligere forskning er også motstridende når det gjelder assosiasjonen mellom PSF og nevropsykologiske faktorer, slik som hjerneslagets lokalisasjon, type og alvorlighetsgrad (3, 8).
Hvordan måles fatigue?
Prevalensen av PSF fra tidligere studier varierer. Tre systematiske oversiktsartikler med 71, 16 og 22 inkluderte studier viser en prevalens på henholdsvis 51–72 prosent (3), 29–70 prosent (12) og 25–35 prosent (13) for PSF. Oversiktsartiklene påpeker at ulike definisjoner av PSF anvendes, og at prevalensmål varierer etter hvilken operasjonalisering av PSF som benyttes.
Det finnes flere måleinstrumenter for å måle fatigue (15), men ingen for fatigue spesifikt etter hjerneslag. Fatigue er en subjektiv opplevelse som bare kan rapporteres av pasienten selv, og derfor benyttes instrumenter for selvrapportering. Ofte benyttes ulike skalaer for å måle PSF, men det finnes ingen fastsatt grense for fatigue (3), noe som kan komplisere tolkningen av data fra denne typen måleinstrumenter.
Hensikten med studien
Årsaken til PSF er uklar, behandlingen er begrenset, og det er betydelig sprik i prevalenstall for PSF (3). Tidligere forskning identifiserer at det tydelig er behov for mer forskning for å sikre pasientene best mulig oppfølging (3, 8, 16). Kunnskap om hvor mange og hvem som strever med PSF, er derfor nødvendig for å kunne tilby disse pasientene målrettet helsehjelp.
Hensikten med denne studien er å undersøke om det er sammenheng mellom fatigue etter hjerneslag og sosiodemografiske, medisinske og kliniske karakteristika i et norsk utvalg.
Metode
Design og utvalg
Denne studien er en tverrsnittsstudie som anvender data fra en randomisert, kontrollert studie (RCT, randomised controlled trial) som undersøkte effekten av en psykososial intervensjon for hjerneslagpasienter (17). Utvalget i tverrsnittsstudien består av pasienter som har hatt hjerneslag, rekruttert fra elleve sykehus i Sørøst-Norge i perioden november 2014 til november 2016.
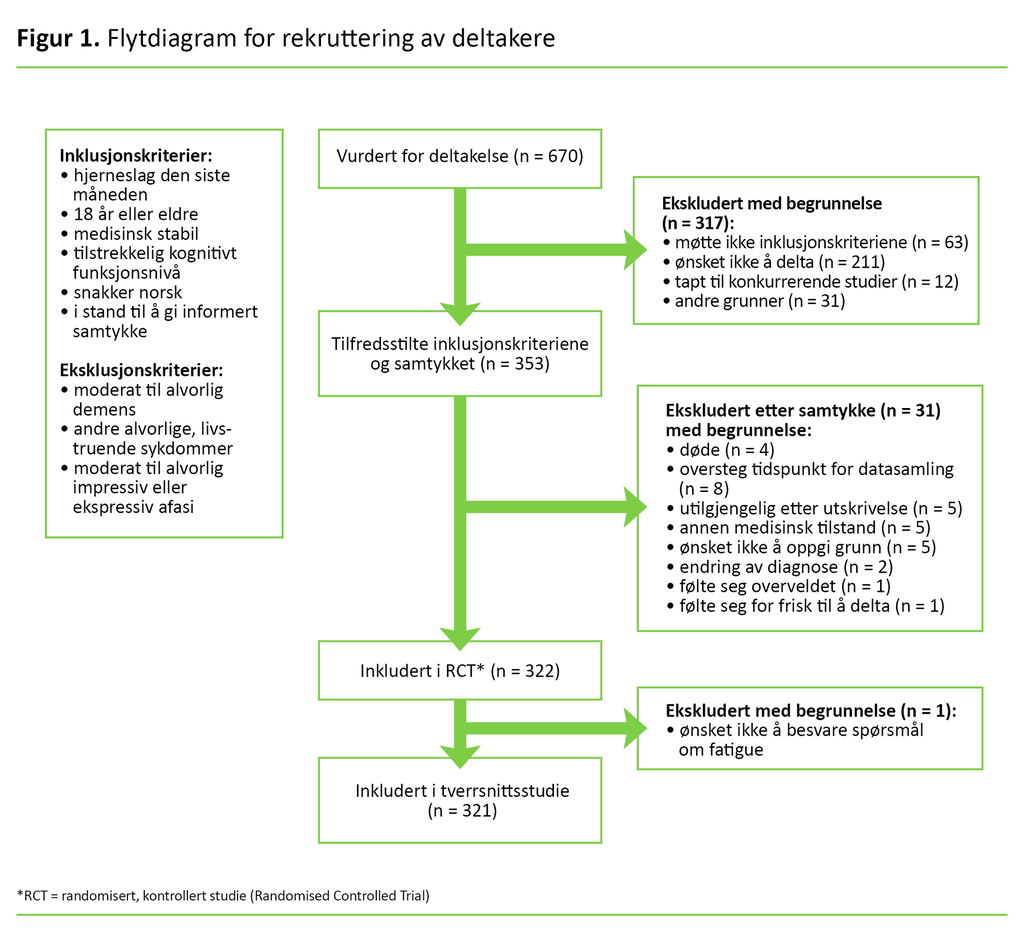
Det var 353 pasienter som oppfylte inklusjonskriteriene og samtykket til å delta i studien (figur 1). Vi registrerte et frafall på 31 deltakere mellom rekrutteringen og datainnsamlingen. Én deltaker unnlot å svare på spørsmål om fatigue, derfor ble totalt 321 deltakere inkludert i tverrsnittsstudien vår.
Datainnsamling og instrumenter
Vi samlet inn datamaterialet 4–6 uker etter hjerneslaget ved å bruke et strukturert spørreskjema i individuelle intervjuer. Spørreskjemaet besto totalt av seks måleinstrumenter (17). Av disse seks måleinstrumentene har vi i denne tverrsnittsstudien kun anvendt ett instrument for å måle fatigue og ett for å måle depresjon. Sykepleiere og ergoterapeuter med opplæring i å bruke måleinstrumentene gjennomførte datainnsamlingen.
I tillegg til data om fatigue og depresjon samlet vi inn data om sosiodemografiske karakteristika som alder, kjønn, sivilstand, bosituasjon, utdanning, omsorgsansvar, arbeidssituasjon før og etter hjerneslaget samt medisinske og kliniske data om hjerneslagets alvorlighetsgrad, hjerneslagtype, hjerneslaglokalisasjon, rehabiliteringstjenester og sykdommer før hjerneslaget.
I denne studien målte vi forekomsten av fatigue og operasjonaliserte PSF ved å bruke en kortversjon av Fatigue Questionnaire (FQ), som består av ett ja/nei-spørsmål: «Føler du deg ofte sliten, uopplagt med mangel på overskudd?» Ved «ja» stilles et oppfølgingsspørsmål om varigheten av symptomene, med svaralternativene «under 1 uke», «under 1 måned», «1–3 måneder», «3–6 måneder» og «6 måneder eller mer» (4, 18).
Nøkkelordene «ofte», «sliten», «uopplagt» og «mangel på overskudd» og den rapporterte varigheten av disse symptomene støtter seg på definisjonen av fatigue som en langvarig og tilbakevendende opplevelse av nedsatt energi og redusert energikapasitet sammenliknet med før hjerneslaget (3).
Vi målte depresjon med Yale-Brown single item screening questionnaire (Yale), som består av ett spørsmål: «Føler du deg ofte trist eller deprimert?», med svaralternativene «ja» og «nei» (19). Yale er et instrument for screening av depresjon som er validert for personer med hjerneslag. Instrumentet er vurdert til å ha tilfredsstillende sensitivitet og spesifisitet sammenliknet med mer omfattende instrumenter for å identifisere depresjon (19).
I akuttfasen på sykehuset vurderte sykehuspersonalet slagets alvorlighetsgrad med National Institutes of Health Stroke Scale (NIHSS). NIHSS består av 11 kliniske observasjoner som tallfestes og summeres på en skala fra 0–42. Høyere sumskår angir høyere grad av funksjonsnedsettelse (20).
Analyse og koding
Vi brukte beskrivende statistikk for å beskrive utvalget i denne studien. Multivariat logistisk regresjonsanalyse ble anvendt med PSF (0 = «nei, ingen rapportert fatigue», 1 = «ja, nylig oppstått fatigue») som den avhengige variabelen. PSF ble operasjonalisert ved «1 = ja» på variabelen FQ dersom fatiguesymptomene nylig var oppstått (<3 måneders varighet). Deltakere som rapporterte om fatiguesymptomer av lengre varighet (>3 måneder) (n = 35), ble ekskludert fra den logistiske regresjonsanalysen.
Basert på tidligere forskning på faktorer som kan være assosiert med PSF (3, 8, 12, 13, 21), inkluderte vi følgende variabler som uavhengige variabler i den logistiske regresjonen: alder ved innleggelse, kjønn (1 = mann), omsorgsansvar for andre (1 = ja), tidligere sykdom (1 = ja), hjerneslagtype (0 = infarkt, 1 = hjerneblødning), alvorlighetsgrad av hjerneslaget (sumskår på NIHSS) og depresjon (1 = ja).
Arbeidssituasjon etter hjerneslaget (0 = i arbeid, 1 = pensjonert/trygdet/arbeidsledig, 2 = sykemeldt) ble inkludert i modellen for å kontrollere for potensiell konfundering. Utvalget for den logistiske regresjonsanalysen inkluderer kun pasienter med komplette medisinske og kliniske data (n = 209). Vi satte signifikansnivået i alle de statistiske analysene til 0,05. Statistiske analyser ble utført i SPSS versjon 25.
Forskningsetiske overveielser
Studien er godkjent av Regionale komiteer for medisinsk og helsefaglig forskningsetikk (REK-nummer 2013/2047) og registrert hos Personvernombudet (registreringsnummer 2014/1026) for de helseforetakene som bidro med å rekruttere til studien. Deltakerne ga frivillig samtykke til å være med i studien og kunne når som helst trekke seg uten begrunnelse eller konsekvenser for videre medisinsk oppfølging.
Resultater
Beskrivelse av utvalget
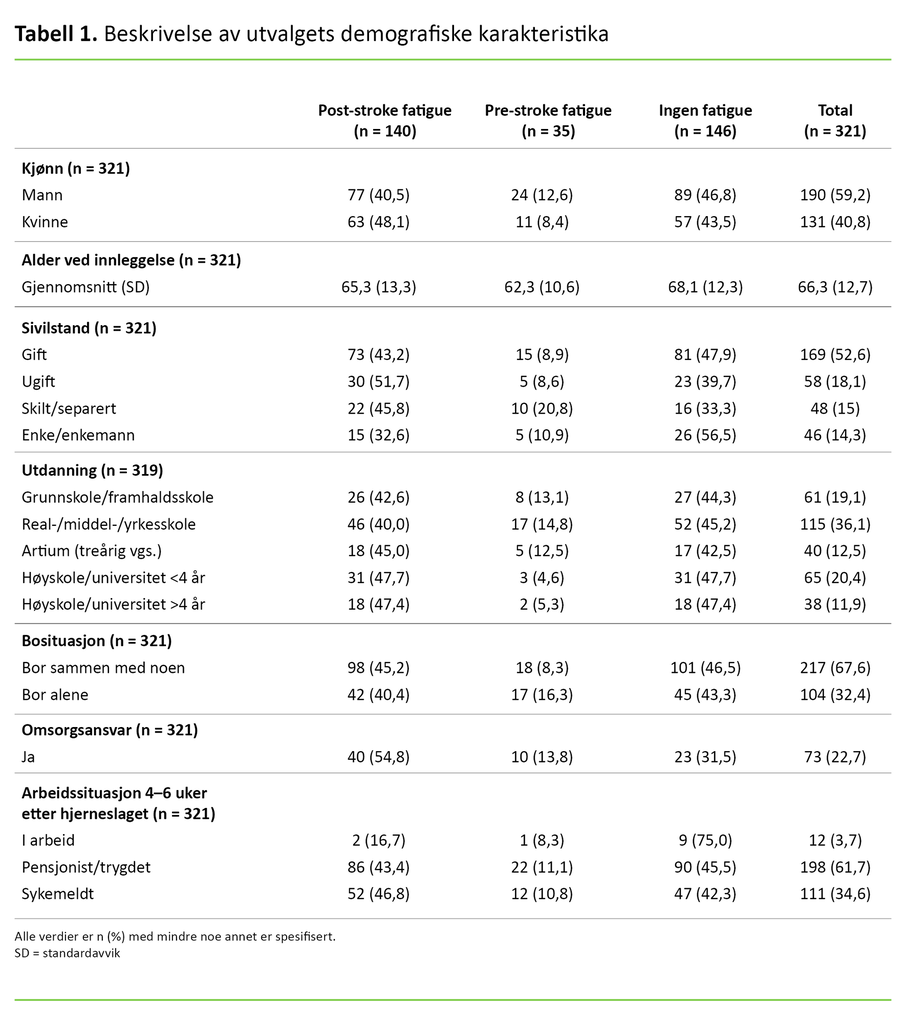
Utvalget i denne studien besto av 59,2 prosent menn og 40,8 prosent kvinner, med en samlet gjennomsnittsalder på 66,3 år. Andelen som hadde omsorgsansvar for egne barn eller andre nærstående, var 22,7 prosent (tabell 1).
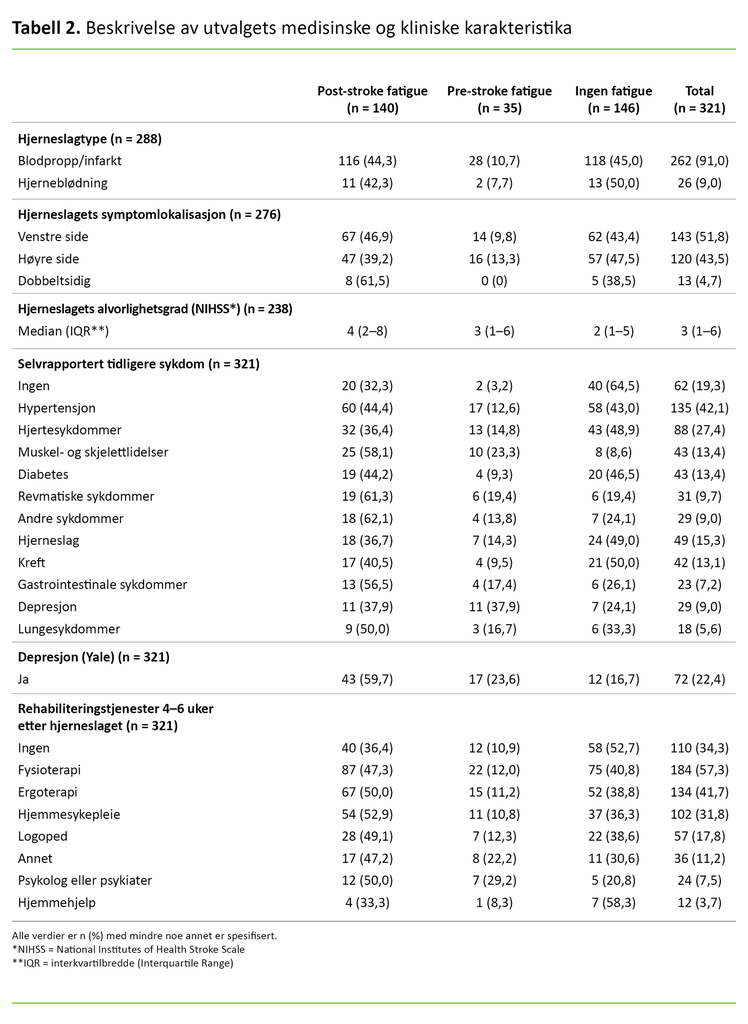
I 91 prosent av tilfellene var blodpropp årsaken til hjerneslaget, mens 9 prosent skyldtes hjerneblødning. Totalt var medianskåren for hjerneslagets alvorlighetsgrad på NIHSS 3, og interkvartilbredden gikk fra 1–6. Kun 19,3 prosent rapporterte ingen tidligere sykdommer. Det var 22,4 prosent som rapporterte om depresjon 4–6 uker etter hjerneslaget. Deltakerne rapporterte at de i utstrakt grad mottok rehabiliteringstjenester 4–6 uker etter hjerneslaget. Kun 34,3 prosent rapporterte at de ikke mottok noen form for rehabiliteringstjenester (tabell 2).
Prevalens og faktorer assosiert med post-stroke fatigue
Prevalensen av PSF var 43,6 prosent. Av dem som rapporterte om PSF, var 55 prosent menn og 45 prosent kvinner, med gjennomsnittsalder på 65,3 år. 10,9 prosent av deltakerne rapporterte om pre-stroke fatigue, altså fatigue før hjerneslaget, mens 45,5 prosent ikke opplevde fatigue 4–6 uker etter hjerneslaget.
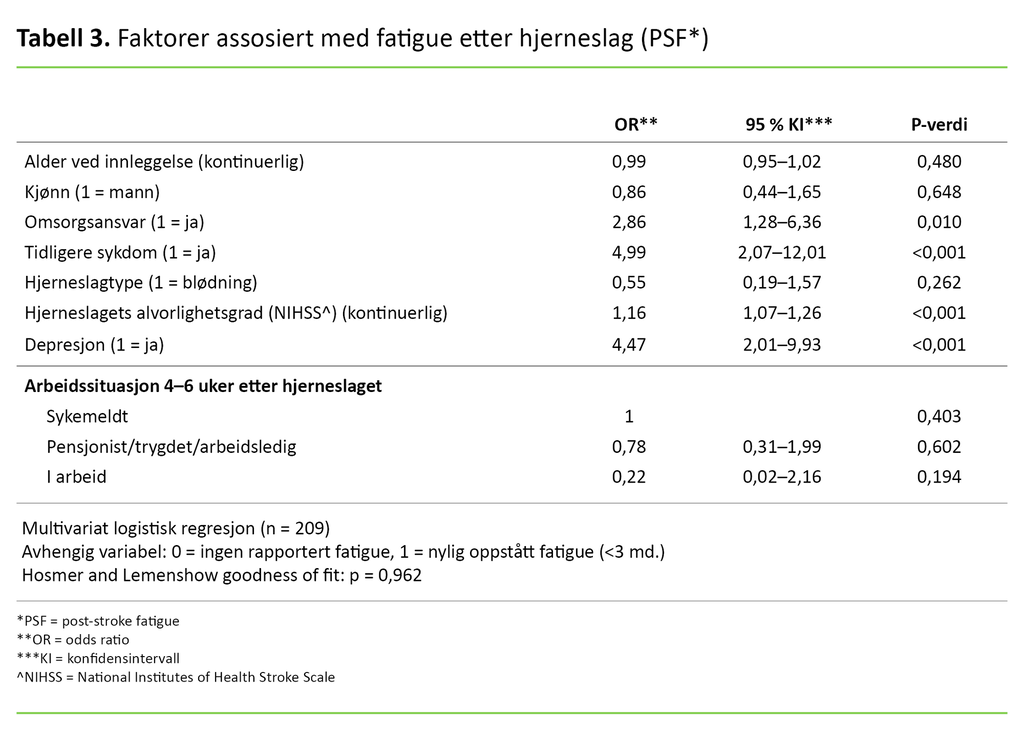
Den logistiske regresjonsanalysen viste at fire faktorer var assosiert med PSF da vi kontrollerte for de andre faktorene i modellen (tabell 3). Pasienter som rapporterte at de hadde tidligere sykdommer før hjerneslaget, hadde nesten fem ganger høyere odds (OR = 4,99; 95 % KI 2,07–12,01; p < 0,001) for å rapportere om PSF sammenliknet med pasienter som ikke rapporterte om tidligere sykdom.
Pasienter som rapporterte om depresjon 4–6 uker etter hjerneslaget, hadde over fire ganger så høy odds (OR = 4,47; 95 % KI 2,01–9,93; p < 0,001) for å rapportere om PSF sammenliknet med pasienter som ikke rapporterte om depresjon. De som hadde omsorgsansvar for andre, hadde over 2,5 ganger høyere odds (OR = 2,86; 95 % KI 1,28–6,36; p = 0,01) for å rapportere om PSF sammenliknet med dem som ikke hadde omsorgsansvar.
For hvert poeng høyere NIHSS-skår hadde pasienten 1,16 ganger høyere odds for å rapportere om PSF (OR = 1,16; 95 % KI 1,07–1,26; p < 0,001). Pasientens kjønn, alder, arbeidssituasjon og slagtype hadde ingen statistisk signifikant assosiasjon med PSF i denne modellen.
Diskusjon
Prevalensen av PSF
Det var 43,6 prosent som rapporterte om PSF 4–6 uker etter hjerneslaget. Dette tallet samsvarer med prevalensen av PSF fra tidligere studier (12, 13). Studier viser at PSF kan være tiltakende over tid. En studie fant at prevalensen av PSF økte fra innleggelsestidspunktet til tre måneder etter hjerneslaget (7). En annen studie viste at prevalensen ved innleggelse, seks og tolv måneder etter hjerneslaget var henholdsvis 52, 64 og 70 prosent (22).
Måletidspunktet 4–6 uker etter hjerneslaget kan forklare den middels til lave prevalensen i vår studie sammenliknet med tidligere studier, men det kan også bety at tidligere studier kan ha brukt andre kriterier for PSF.
Definisjonen av PSF er ikke entydig i forskningslitteraturen, og det finnes ingen spesifikke måleinstrumenter for PSF (3). At det foreligger store prevalenssprik for PSF fra tidligere studier (3), kan skyldes at begrepet «post-stroke fatigue» er definert og operasjonalisert forskjellig.
Fatigue betegnes ofte som tretthet eller mangel på energi, som er assosiert med både biologiske, psykologiske og sosiale faktorer (11). Tidligere studier presiserer at begrepet PSF burde defineres mer enhetlig ved for eksempel å skille mellom fysisk og mental fatigue (23). Prevalensen av PSF kan se ut til å være noe lavere i for eksempel Asia (35 prosent) enn i Europa (13), noe som indikerer at sosiale faktorer kan henge sammen med opplevelsen av fatigue.
Andre sykdommer før hjerneslaget økte oddsen for PSF
I denne studien fant vi at det å rapportere om andre sykdommer før hjerneslaget ga nesten fem ganger høyere odds for å rapportere om PSF. Foreløpig er det ikke godt nok utforsket hvilke typer sykdommer som kan predikere PSF, men både depresjon og pre-stroke fatigue er faktorer som har vist seg å ha sammenheng med PSF (24, 25). Det har lenge vært kjent at premorbide faktorer kan ha sammenheng med PSF.
En studie fra 2005 fant at pre-stroke fatigue var den faktoren som ga høyest odds for å oppleve PSF, men at også høyere alvorlighetsgrad på hjerneslaget og opplevd depresjon etter hjerneslaget var blant de viktigste faktorene for å oppleve PSF (24). At både høyere alvorlighetsgrad på hjerneslaget og depresjon etter hjerneslaget viste sammenheng med PSF, samsvarer med våre funn.
Pre-stroke fatigue kan være en viktig faktor for PSF, men studien vår viser ikke et signifikant funn om at pre-stroke fatigue har sammenheng med PSF, da vi ikke målte pre-stroke fatigue som en egen faktor.
Høyere alvorlighetsgrad på hjerneslaget ga høyere odds for PSF
Tidligere forskning tyder på liten sammenheng mellom alvorlighetsgrad og PSF (3). Funn fra vår studie viste at slagets alvorlighetsgrad var en signifikant faktor som økte oddsen for PSF, hvor hvert poeng høyere på NIHSS økte oddsen for PSF med 1,16. Flere tidligere studier trekker imidlertid i liten grad frem at medisinske og kliniske faktorer er viktige for opplevelsen av PSF (3, 8).
En norsk systematisk litteraturgjennomgang konkluderte med at hjerneslagets alvorlighetsgrad har ingen eller tvilsom assosiasjon til PSF; det var ingen av de inkluderte studiene i denne systematiske litteraturgjennomgangen som fant noen signifikant sammenheng mellom hjerneslagets alvorlighetsgrad og PSF (3). På den annen side fant en studie at slagets alvorlighetsgrad viste seg å være en faktor som hadde signifikant sammenheng med PSF (24).
Disse motstridende funnene kan skyldes ulikheter i studienes design, operasjonalisering av fatigue eller utvalgsstørrelsen. Funnene i vår studie indikerer at høyere alvorlighetsgrad på hjerneslaget kan ha betydning for PSF. Hjerneslagtype har usikker assosiasjon til PSF (3), og vi fant heller ingen sammenheng mellom hjerneslagtype og PSF i vår studie.
Depresjon var sterkt assosiert med PSF
Resultatene i denne studien viste en sterk sammenheng mellom opplevd fatigue og depresjon 4–6 uker etter hjerneslaget. Det var over fire ganger høyere odds for å rapportere om PSF dersom man også rapporterte om depresjon på samme tidspunkt. Dette funnet samsvarer godt med tidligere forskning, som har vist at depresjon er utbredt hos dem som opplever PSF (14, 26, 27).
Det var totalt 22,4 prosent som rapporterte om depresjon. Andelen som samtidig rapporterte om PSF, var 59,7 prosent, og forekomsten var kun 16,7 prosent blant dem som ikke rapporterte om PSF. Det er formodentlig en sammensatt forklaring på hvorfor depresjon forekom så ofte sammen med fatigue. Fatigue og depresjon er trolig ulike deler av samme spektrum med liknende årsaksforklaringer (11).
Nedsatt energi inngår ofte som et kriterium i ulike definisjoner og målinger av depresjon. Det er derfor mulig at instrumentene måler ulike deler av et fenomen i samme domene. En del av samvariasjonen kan delvis være uttrykk for lingvistiske utfordringer i måleinstrumentene. Fatigue kjennetegnes av reduserte muligheter til å utføre daglige gjøremål, som igjen kan føre til depresjon og svekket livskvalitet (9).
Tilstanden fatigue kan også påvirkes av at pasienten er redd for fremtidsutsiktene, eller noen pasienter kan i utgangspunktet være mer sårbare for å oppleve PSF på grunn av sykdom før hjerneslaget. Både depressive symptomer og pre-stroke fatigue er faktorer som er funnet å kunne være relatert til PSF (25).
Det er interessant å se på sammenhenger med pasientens helse før hjerneslaget og PSF opp mot funnene i denne studien. Funnene viste at forekomsten av depresjon etter hjerneslaget var høyere blant dem som rapporterte at de opplevde fatigue også før hjerneslaget, sammenliknet med dem som ikke rapporterte om fatigue etter hjerneslaget. Men forekomsten av depresjon etter hjerneslaget var høyest blant dem som rapporterte at de opplevde fatigue mer nylig etter hjerneslaget (tabell 2). Det er et utydelig skille mellom de tre fenomenene fatigue, depresjon og angst etter et hjerneslag (14).
Sammenheng mellom livssituasjon og PSF
PSF kan ha en viktig sammenheng med psykososiale faktorer. I studien vår fant vi at det å ha omsorgsansvaret for andre, var en signifikant faktor som økte oddsen for å oppleve PSF. At omsorgsansvar for andre var assosiert med PSF, kan forklares med at det er belastende å ivareta seg selv i en akutt sykdomsfase og samtidig ha omsorgsansvaret for andre personer, enten for barn, ektefelle eller andre nærstående.
Denne assosiasjonen indikerer at PSF burde ses i sammenheng med slagrammedes livssituasjon (21). Arbeidssituasjon hadde for øvrig ingen betydning for opplevelsen av PSF for utvalget i studien vår.
Betydningen av alder for opplevelsen av PSF er tidligere undersøkt, men sammenhengen er uklar (3). En studie fant at eldre opplever PSF oftere enn unge (22), og det er også funnet at forekomsten var høyere blant yngre slagrammede (28). Funnene våre viser ingen sammenheng med alder.
Det at tidligere sykdommer før hjerneslaget, og det at hjerneslagets alvorlighetsgrad økte oddsen for PSF i denne studien, peker mot at biologiske faktorer kan øke oddsen for PSF. En sosial faktor som å ha omsorgsansvaret for andre samt opplevd depresjon etter hjerneslaget økte oddsen for PSF. Dette viser at PSF kan være et sammensatt fenomen. Det er uklart om PSF først og fremst har en medisinsk årsaksforklaring, eller om det er psykososiale faktorer og omgivelser rundt pasienten som bidrar til opplevelsen av PSF (11).
Styrker og begrensninger ved studien
Operasjonalisering av fatigue
Instrumentet og spørsmålsformuleringen vi har valgt til å operasjonalisere fatigue, legger føringer for hvordan PSF tolkes i denne studien. Det kan være vanskelig å velge ett svaralternativ på strukturerte spørreskjemaer, noe som kan ha ført til over- eller underrapportering. Spørsmålsformuleringen kan i sin tur ha betydning for om hvorvidt PSF måles korrekt i forhold til hvordan fenomenet faktisk arter seg for pasienten.
Måten vi definerte varigheten på fatigue-symptomene på, kan være en svakhet ved studien vår, da svaralternativene som pasienten fikk, ikke avgrenser nøyaktig til «før» eller «etter» hjerneslaget. Vi kunne oppnådd større nøyaktighet dersom svaralternativene om varigheten hadde vært flere.
Definisjon og operasjonalisering av begrepet PSF kan være en utfordring i og med at det ikke finnes et validert instrument for å måle fenomenet PSF, altså fatigue etter et hjerneslag. PSF kan arte seg annerledes i andre sammenhenger enn etter et hjerneslag. I studien vår var det hensiktsmessig å skille ut pasientene som rapporterte tydelig om langvarig fatigue (>3 måneder), i og med at vi ville undersøke fatigue som oppsto etter hjerneslaget. Vi kan ikke utelukke at de som rapporterte om fatigue med lengre varighet, tolket spørsmålet om fatigue på samme måte som dem som opplevde nylig oppstått fatigue. Vi kan heller ikke utelukke at resultatene hadde blitt annerledes dersom vi hadde brukt andre instrumenter.
Selv om det fortsatt er usikkert hvordan PSF best kan måles, kan denne studien bidra til ny kunnskap om hvem som opplevde fatigue 4–6 uker etter hjerneslaget, og dermed hvem som kan være i risiko for å få nedsatt livskvalitet etter hjerneslag (6, 9, 10).
De rapporterte konfidensintervallene (95 % KI) fra den logistiske regresjonsanalysen (tabell 3) er relativt brede. Variasjonsbredden skyldes sannsynligvis at et lite utvalg gir større variasjon rundt det sanne estimatet. Det innebærer at selv om resultatene er statistisk signifikante, vil den estimerte oddsratioen for hver av variablene måtte tolkes med forsiktighet.
Utvalgets representativitet
Det var utfordringer med å følge rekrutteringsprotokollen ved hvert sykehus. Det kan ha bidratt til at enkelte pasienter som oppfylte inklusjonskriteriene, ikke har blitt forespurt om å delta, noe som kan ha ført til utilsiktede skjevheter i utvalget. Noen pasienter ønsket ikke å være med i studien, blant annet fordi de følte seg for syke. De pasientene som hadde mer alvorlige utfall og mer uttalt fatigue, kan ha valgt ikke å delta i studien fordi de anså det som for krevende.
En annen begrunnelse for at pasienter ikke ville delta i denne studien, var at de følte seg for friske. Når pasienter føler seg for syke til å delta i en studie, kan det føre til at vi får en skjevhet i utvalget, eller at det er de friskeste som er representert i studien. Sammenliknet med populasjonen som er registrert i hjerneslagregisteret (29), er deltakerne i studien vår i gjennomsnitt 10 år yngre. Andelen kvinner er 5 prosent lavere, og andelen med lette hjerneslag (NIHSS <6) er 5 prosent høyere.
Datainnsamling med strukturert spørreskjema i individuelle intervjuer kan senke pasientens terskel for å gjennomføre spørreskjemaet, noe som gir større gjennomføringsprosent. En slik tilnærming bidrar til å samle mer komplette data og forhindrer manglende data. I tillegg reduseres muligheten for å misforstå spørreskjemaet.
En av styrkene ved denne studien er at den benytter data fra en multisenterstudie som har rekruttert pasienter fra flere forskjellige sykehus i landet. Videre inkluderer vi et stort antall deltakere i studien. Disse momentene øker resultatenes generaliserbarhet til hjerneslagpasienter for øvrig.
Konklusjon
I studien vår var forekomsten av fatigue hos pasienter 4–6 uker etter hjerneslag 43,6 prosent. Følgende faktorer økte oddsen for PSF i utvalget: tidligere sykdommer før hjerneslaget, opplevelse av depresjon etter hjerneslaget, omsorgsansvar for andre nærstående samt høyere alvorlighetsgrad på hjerneslaget (målt med NIHSS).
Sykepleiere og helsepersonell trenger å vite hvem som er spesielt sårbare for å oppleve PSF, slik at disse pasientene kan få riktig oppfølging til riktig tid. Da er det viktig å vite hvor stor forekomsten av PSF er, og hvilke faktorer som assosieres med PSF. Det er imidlertid behov for mer forskning på PSF.
Takk til statistiker Manuela Zucknick på Avdeling for biostatistikk ved Universitetet i Oslo for hjelp til å kvalitetssikre statistiske analyser og fortolkninger.
Studien vår er finansiert med støtte fra Helse Sør-Øst (prosjektnummer 2013086) og Den europeiske unions sjuende rammeprogram (FP7-PEOPLE-2013-COFUND) (avtalenummer 609020 – Scientia Fellows). Universitetet i Oslo og Oslo universitetssykehus, Ullevål har bidratt med forskningstid og administrativ støtte til å gjennomføre studien.
Referanser
1. Ellekjær H, Selmer R. Hjerneslag – like mange rammes, men prognosen er bedre. Tidsskr Nor Legeforen. 2007;127:740–3.
2. Kirkevold M, Christensen D, Andersen G, Johansen S, Harder I. Fatigue after stroke: manifestations and strategies. Disabil Rehabil. 2012;34(8):665–70.
3. Schillinger A, Becker F. Fatigue/utmattelse etter traumatisk hjerneskade og hjerneslag. Tidsskr Nor Legeforen. 2015;135:331–5.
4. Loge JH, Ekeberg O, Kaasa S. Fatigue in the general Norwegian population: normative data and associations. J Psychosom Res. 1998;45(1):53–65.
5. Elf M, Eriksson G, Johansson S, von Koch L, Ytterberg C. Self-reported fatigue and associated factors six years after stroke. PLoS One. 2016;11(8):e0161942.
6. Lerdal A, Gay CL. Fatigue in the acute phase after first stroke predicts poorer physical health 18 months later. Neurology. 2013;81(18):1581–7.
7. Delva II, Lytvynenko NV, Delva MY. Post-stroke fatigue and its dimensions within first 3 months after stroke. Wiad Lek. 2017;70(1):43–6.
8. Ponchel A, Bombois S, Bordet R, Hénon H. Factors associated with poststroke fatigue: a systematic review. Stroke Res Treat. 2015;2015:347920.
9. Mandliya A, Das A, Unnikrishnan JP, Amal MG, Sarma PS, Sylaja PN. Post-stroke fatigue is an independent predictor of post-stroke disability and burden of care: a path analysis study. Top Stroke Rehabil. 2016;23(1):1–7.
10. Wu S, Barugh A, Macleod M, Mead G. Psychological associations of poststroke fatigue: a systematic review and meta-analysis. Stroke. 2014;45(6):1778–83.
11. Ormstad H, Eilertsen G. A biopsychosocial model of fatigue and depression following stroke. Medical Hypotheses. 2015;85(6):835–41.
12. Nadarajah M, Goh HT. Post-stroke fatigue: a review on prevalence, correlates, measurement, and management. Top Stroke Rehabil. 2015;22(3):208–20.
13. Cumming TB, Packer M, Kramer SF, English C. The prevalence of fatigue after stroke: A systematic review and meta-analysis. Int J Stroke. 2016;11(9):968–77.
14. Galligan NG, Hevey D, Coen RF, Harbison JA. Clarifying the associations between anxiety, depression and fatigue following stroke. J Health Psychol. 2015;21(12):2863–71.
15. Mead G, Lynch J, Greig C, Young A, Lewis S, Sharpe M. Evaluation of fatigue scales in stroke patients. Stroke. 2007;38(7):2090–5.
16. Kutlubaev MA, Mead GE, Lerdal A. Fatigue after stroke – perspectives and future directions. Int J Stroke. 2015;10(3):280–1.
17. Kirkevold M, Bragstad LK, Bronken BA, Kvigne K, Martinsen R, Gabrielsen EH, et al. Promoting psychosocial well-being following stroke: study protocol for a randomized, controlled trial. BMC Psychol. 2018;3(1):12.
18. Chalder T, Berelowitz G, Pawlikowska T, Watts L, Wessely S, Wright D, et al. Development of a fatigue scale. J Psychosom Res. 1993;37(2):147–53.
19. Watkins C, Lightbody C, Sutton C, Holcroft L, Jack C, Dickinson H, et al. Evaluation of a single-item screening tool for depression after stroke: a cohort study. Clin Rehabil. 2007;21(9):846–52.
20. Adams Jr HP, Davis PH, Leira EC, Chang K-C, Bendixen BH, Clarke WR, et al. Baseline NIH Stroke Scale score strongly predicts outcome after stroke. Neurology. 1999;53(1):126–31.
21. Martinsen R, Kirkevold M, Sveen U. Younger stroke survivors' experiences of family life in a long-term perspective: a narrative hermeneutic phenomenological study. Nurs Res Pract. 2012;2012(Article ID 948791):11.
22. Schepers VP, Visser-Meily AM, Ketelaar M, Lindeman E. Poststroke fatigue: course and its relation to personal and stroke-related factors. Arch Phys Med Rehabil. 2006;87(2):184–8.
23. Hubacher M, Calabrese P, Bassetti C, Carota A, Stöcklin M, Penner I-K. Assessment of post-stroke fatigue: the fatigue scale for motor and cognitive functions. Eur Neurol. 2012;67(6):377–84.
24. Choi-Kwon S, Han SW, Kwon SU, Kim JS. Poststroke fatigue: characteristics and related factors. Cerebrovasc Dis. 2005;19(2):84–90.
25. Lerdal A, Bakken LN, Rasmussen EF, Beiermann C, Ryen S, Pynten S, et al. Physical impairment, depressive symptoms and pre-stroke fatigue are related to fatigue in the acute phase after stroke. Disabil Rehabil. 2011;33(4):334–42.
26. Kim JS. Post-stroke mood and emotional disturbances: pharmacological therapy based on mechanisms. J Stroke. 2016;18(3):244–55.
27. Kouwenhoven SE, Kirkevold M, Engedal K, Kim HS. Depression in acute stroke: prevalence, dominant symptoms and associated factors. A systematic literature review. Disabil Rehabil. 2011;33(7):539–56.
28. Lerdal A, Gay C, Lee K. Curvilinear relationship between age and post-stroke fatigue among patients in the acute phase following first-ever stroke. Int J Phys Med Rehabil. 2013;1(5).
29. Fjærtoft H, Indredavik B, Mørch B, Phan A, Skogseth-Stephani R, Varmdal R. Årsrapport 2016 – med plan for forbedringstiltak. 2017; St. Olavs hospital HF: Nasjonalt sekretariat for Norsk hjerneslagregister, Seksjon for medisinske kvalitetsregistre, Norsk Hjerneslagregister. Tilgjengelig fra: https://stolav.no/Medisinskekvalitetsregistre/Norsk-hjerneslagregister/%C3%85rsrapport2016-Norsk-hjerneslagregister.pdf (nedlastet 13.10.2018).
Mest lest
Doktorgrader
Kort- og langsiktige følger etter distal dyp venetrombose og overfladisk venetrombose i underekstremitetene
Fødende kvinner vil ha ekte personlig omsorg
Korleis kan jordmor balansera etiske vurderingar om helsa til fosteret opp mot gravide kvinners autonomi og ønskjer i forhold til fosterovervaking?
Dokumentering av de udokumenterte – bruk av svangerskapsomsorg og perinatale utfall blant udokumenterte migranter i Norge



















Kommentarer