Covid-19 og håndtering og stell av perifere venekatetre
Bakgrunn: Under covid-19-pandemien gjennomførte sykehusene en rekke smitteverntiltak som kunne påvirke kvaliteten på innleggelsen og håndteringen av perifere venekatetre (PVK). Studier gjennomført før pandemien fant en høy andel av komplikasjoner knyttet til PVK, men så langt har ingen studier vurdert kvaliteten under perioden med pandemi.
Hensikt: Denne prospektive studien tok sikte på å undersøke hvilken effekt pandemien hadde på håndtering og stell av PVK.
Metode: Det ble innhentet data fra voksne pasienter (> 18 år) på et universitetssykehus i Norge over en treukers periode i februar 2020 (før pandemien: FP-gruppen) og en treukers periode i oktober 2020 (under pandemien: P-gruppen). Det primære utfallsmålet var kvaliteten på PVK slik den ble fastsatt av det validerte spørreskjemaet PVK-miniQ, som består av 16 påstander vedrørende avvik fra beste praksis.
Resultat: Studien omfattet 483 PVK-er og 413 pasienter. Av disse ble 238 PVK-er (49,3 prosent) innhentet fra FP-gruppen og 245 (50,7 prosent) fra P-gruppen. I FP-gruppen var 41,8 prosent av PVK‑ene størrelse 18 (grønt PVK) eller større, sammenliknet med 53,3 prosent i P-gruppen. Median skår på PVK-miniQ var 2 i begge gruppene, med en variasjonsbredde på 0–10 i FP-gruppen og 0–8 i P-gruppen. Forbedret kvalitet i form av færre pasienter som rapporterte om smerte, ble registrert i P-gruppen (14,3 prosent sammenliknet med 6,7 prosent), og 36,3 prosent hadde blod i IV-slangen i FP-gruppen, sammenliknet med 26,5 prosent i P-gruppen. I P-gruppen ble det imidlertid dårligere kvalitet for spørsmålene i PVK-miniQ om henholdsvis pussdannelse (0 prosent i FP-gruppen, sammenliknet med 6 prosent i P-gruppen) og løsnet bandasje (15,2 prosent i FP-gruppen sammenliknet med 24,9 prosent i P-gruppen). Dokumentasjonen av innleggelsen av PVK og indikasjonen var like mangelfull i begge gruppene (p = 0,857).
Konklusjon: Selv om det ble funnet forskjeller på enkelte påstander (items), forble kvaliteten på PVK slik den ble målt av PVK-miniQ, uendret under pandemien. Gitt den lave arbeidsbelastningen på vårt sykehus under pandemien, er det et paradoks at stellet av PVK ikke ble forbedret.
Referer til artikkelen
Helland E, Høvik L, Gustad L, Gjeilo K. Covid-19 og håndtering og stell av perifere venekatetre. Sykepleien Forskning. 2024; 19(95645):e-95645. DOI: 10.4220/Sykepleienf.2024.95645
Introduksjon
Innleggelse av perifert venekateter (PVK) er en av de hyppigst utførte invasive prosedyrene hos sykehuspasienter og er forbundet med en risiko for komplikasjoner, som problemer med innstikket, dislokasjon, infiltrasjon, okklusjon, flebitt og blodbaneinfeksjon (1–6).
Kliniske tegn på innstikksstedet som ofte benyttes ved vurdering av flebitt, er smerter, rødhet, ødem, varme, pussdannelse, strek/rød linje langs venen, hardt vev og palpabel venestreng (7). En blodbaneinfeksjon forårsaket av et PVK betraktes som den mest alvorlige av alle sykehusinfeksjoner, og ble i 2019 rangert som en av de ti viktigste risikoene for pasientsikkerheten (8, 9).
Sykehusinfeksjoner kan føre til langvarige sykehusopphold, økt morbiditet og mortalitet, mer bruk av antibiotika og økte offentlige helseutgifter (1, 8, 9). I en systematisk oversiktsartikkel fra 2017 ble det funnet at 22 prosent av alle blodbaneinfeksjoner forårsaket av venekatetre var knyttet til PVK (4), og i Spania har det blitt påvist at blodbaneinfeksjoner forårsaket av PVK øker i generelle sykehusavdelinger (10).
I Norge står primære blodbaneinfeksjoner for 7 prosent av alle sykehusinfeksjoner (11). En norsk studie fant at rundt 8 prosent av alle blodbaneinfeksjoner forårsaket av S. aureus stammet fra et venekateter, mens 25 prosent stammet fra en ukjent kilde (12), som kan ha vært et PVK.
Størrelsen på PVK, innstikksstedet, antallet PVK som legges inn, festing av bandasjen, mangel på dokumentasjon og den tiden PVK sitter inne, er forbundet med risiko for komplikasjoner (13). Internasjonale retningslinjer anbefaler at man unngår å legge PVK inn i anatomiske områder med fleksjon, og at man velger et PVK av en størrelse som er tilpasset den tiltenkte bruken (14). Et PVK bør være stabilisert med en steril, ren, tørr og intakt bandasje (13). Dato for innleggelsen bør være dokumentert både på bandasjen og i pasientjournalen (1).
PVK som er i bruk, bør skiftes bare etter klinisk indikasjon (15, 16), og PVK som ikke har noen hensikt, bør fjernes raskt (14). Komplikasjoner fra PVK kan forebygges ved å følge kunnskapsbaserte trinn som sikrer at beste praksis følges ved innleggelsen og håndtering av PVK. Dette omfatter daglig vurdering av PVK-et og innstikksstedet, med klinisk vurdering av komplikasjoner og overholdelse av retningslinjene for smittevern (13, 16–18).
Covid-19-pandemien ga opphav til et naturlig eksperiment, med nye krav som kunne ha påvirket kvaliteten av PVK, inkludert krav til smittevern, bruk av personlig beskyttelsesutstyr, mindre mulighet til å skille rene soner fra urene, og mentale og etiske påkjenninger som kunne ha påvirket kvaliteten på arbeidet generelt (19–21).
Hovedformålet med denne studien var å bruke det validerte spørreskjemaet PIVC Mini Questionnaire (PVK-miniQ) (22) til å vurdere overholdelsen av kunnskapsbaserte anbefalinger om håndtering og stell av PVK ved et norsk sykehus under den første pandemibølgen, sammenliknet med en undersøkelse gjennomført før pandemien.
Metode
Design
Kvaliteten på stellet av PVK ble målt prospektivt ved å bruke spørreskjemaet PVK-miniQ (22) i to ikke-annonserte tverrsnittsundersøkelser. Den første av disse ble gjennomført i februar/mars 2020 (før pandemien: FP-gruppen), og den andre i oktober/november 2020 (under pandemien: P-gruppen).
Studien omfattet kun PVK, og kvaliteten på midlinekatetre og perifert innlagte sentralkatetre ble derfor ikke målt. Undersøkelsene ble gjennomført i uke 9, 10 og 11 i 2020 i FP-gruppen, og i uke 43, 44 og 45 i P-gruppen.
Deltakere og setting
Studien ble gjennomført i et norsk universitetssykehus med rundt 1000 sengeplasser. Det er et lokalsykehus for 327 000 mennesker og tjener som henvisningssykehus for 730 000 innbyggere.
For hver av undersøkelsene ble det rekruttert et bekvemmelighetsutvalg av voksne pasienter (> 18 år) som var innlagt på en medisinsk eller kirurgisk avdeling eller en intensivenhet. Dette dekket alle 14 avdelinger og enheter. Alle pasienter som var tilgjengelige på sin avdeling på tidspunktet for screeningen, ble inkludert, med unntak av pasienter som var ute av stand til å motta informasjon eller gi muntlig samtykke.
Under covid-19-pandemien ble screeningen foretatt i henhold til en standardprosedyre (SOP) utviklet for å motvirke risikoen for å overføre covid-19 under datainnsamlingen. Personer som var diagnostisert med covid-19, ble ikke inkludert i studien på grunn av begrensninger på bruk av smittevernutstyr.
Datainnsamling
Prosjektlederen og sykepleiere fra sykehusets smittevernavdeling ledet prosjektet og samlet inn data ved å bruke PVK-miniQ sammen med fagutviklingssykepleiere. Screeningene ble gjennomført på ukedager etter klokken 11.00 for å sikre at pasientene ikke var opptatt med frokost eller legevisitt. For å unngå å øke oppmerksomheten rundt håndteringen av PVK ble det nøyaktige tidspunktet for datainnsamlingen ikke bekjentgjort for personalet på de avdelingene screeningen ble foretatt.
Observasjon av hvert PVK mens PVK-miniQ ble fylt ut, tok vanligvis 3–4 minutter, og pasientjournalene ble sjekket for indikasjon og dokumentasjon av PVK umiddelbart etter observasjonen. På grunn av smitteverntiltakene under pandemiperioden insisterte avdelingene på at deres egne sykepleiere skulle gjennomføre PVK-undersøkelsen i P-gruppen. I FP‑gruppen ble målingene derimot foretatt av sykepleiere som hadde fått opplæring i hvordan undersøkelsen skulle gjennomføres.
Detaljer i PVK-miniQ
PVK-miniQ evaluerer håndtering og stell av PVK (22) i tråd med anbefalinger i internasjonal kunnskapsbasert litteratur og retningslinjer for beste praksis (18), og har blitt validert i to land (22, 23). En engelsk versjon av PVK-miniQ er tidligere publisert (22), se Additional file 1, figure S1. I en tidligere studie var intraklassekorrelasjonen (ICC) mellom 64 norske observatører 0,678 på ett sykehus og 0,577 på et annet (22).
PVK-miniQ består av to deler (22). Den første delen inneholder generell informasjon om pasientens alder og kjønn, tiden PVK har sittet inne, størrelsen på PVK, innstikkssted og kontekst for innleggelsen (prehospitalt, akuttmottak, operasjonsavdeling, sengepost/intensivavdeling eller under computertomografi (CT) / magnetisk resonanstomografi (MR)).
Den andre delen angir 16 kliniske observasjoner. Av disse er 8 observasjoner av kliniske tegn på komplikasjoner på innstikksstedet (det vil si smerter, rødhet, ødem, varme, pussdannelse, rød strek/linje langs venen, hardt vev og palpabel venestreng), og disse summeres opp til en skår for flebitt (kontinuerlig skår fra 0 til 8 tegn på flebitt). Ett tegn på flebitt var nok til å kategorisere observasjonen som flebitt, og høyere skårer var tegn på at det forekom flere tegn på flebitt.
De resterende 8 observasjonene var knyttet til bandasjer/utstyr, dokumentasjon og indikasjon for PVK. Hver av disse 16 observasjonene er enten til stede (1 poeng) eller fraværende (0 poeng). Det kan beregnes en samlet skår fra 0 til 16 for hvert PVK, der en høyere skår betyr økende avvik fra beste praksis for håndtering og stell av PVK.
PVK-miniQ ble skrevet ut i et maskinlesbart format. Det ble fylt ut ett skjema for hvert PVK, og skjemaene ble skannet ved en enhet for klinisk forskning ved det lokale universitetet.
Forskningsetikk
Denne studien ble betraktet som et helsekvalitetsprosjekt, og det ble ikke samlet inn direkte identifiserbar pasientinformasjon. Norsk senter for forskningsdata (NSD), nå kalt Sikt – Kunnskapssektorens tjenesteleverandør, anså derfor at informert muntlig samtykke var tilstrekkelig under gjeldende norsk lovgivning. Deltakerne ga muntlig samtykke til screeningen og innsamling av informasjon fra deres pasientjournal.
Studien ble godkjent av sykehusets medisinske direktør og er i henhold til retningslinjene for kvalitetsforbedringsstudier. En vurdering av personvernkonsekvenser var ikke påkrevet, ettersom risikoen ved å behandle anonyme persondata er minimal.
Analyse
For å belyse problemstillingen ble det utført deskriptive og sammenliknende analyser. Kategoriske data ble rapportert som frekvenser (n) og prosentandeler (%), og kontinuerlige data som median (variasjonsbredde) og/eller gjennomsnitt (standardavvik – SD) etter hva som var hensiktsmessig. Det ble gjort en univariat analyse av kategoriske data for å beskrive frekvenser og prosentandeler. Siden kvinner er mer tilbøyelig til å rapportere smerter ved flebitt (6), sjekket vi fordelingen av menn og kvinner i både før-pandemigruppen og pandemigruppen.
Fordelingen av kontinuerlige data ble kontrollert ved å bruke Kolmogorov-Smirnovs test for normalitet, histogrammer og et Q-Q-plott. Det ble oppdaget at dataene var skjevt fordelt, og Mann-Whitneys U-test ble derfor benyttet til å sammenlikne kontinuerlige totalskårer mellom den første og den andre undersøkelsen. Kategoriske data ble sammenliknet med bruk av Pearsons khikvadrattest eller Fischer-Freeman-Haltons eksakte test ut fra hva som var hensiktsmessig for antallet i hver celle.
Vi testet forskjellene i dokumentasjon og indikasjon for PVK mellom FP- og P-gruppen for hver innleggelseskontekst (prehospitalt, akuttmottak, sengepost/intensivavdeling, ukjent, generelt). Dette ble gjort ved å slå sammen andelene (%) av manglende data om PVK, manglende dokumentasjon i pasientjournalen og indikasjonen for bruk i hver innleggelseskontekst for FP- og P-gruppen. Denne tilnærmingen reduserte antallet statistiske tester fra 18 til 6, noe som reduserte sannsynligheten for falskt positive funn.
For alle sammenlikningene ble en tosidig verdi < 0,05 ansett som statistisk signifikant. Analysene av data ble foretatt i IBM SPSS Statistics versjon 27 og STATA/SE versjon 17.0.
Resultater
Vi kontaktet 413 pasienter, og alle samtykket i å delta i studien. Som vist i tabell 1, ble PVK‑miniQ benyttet til å observere totalt 483 PVK-er hos 413 pasienter. FP-gruppen omfattet 238 (49,3 prosent) PVK-er hos 199 (48,2 prosent) pasienter, og P-gruppen omfattet 245 (50,7 prosent) PVK-er hos 214 (51,8 prosent) pasienter. Alder (p = 0,791) og antallet kateterdager (p = 0,244) var likt i de to gruppene. Prosentandelen menn (59,8 prosent) i forhold til kvinner (40,2 prosent) var høyere i FP-gruppen enn i P-gruppen (p = 0,002).
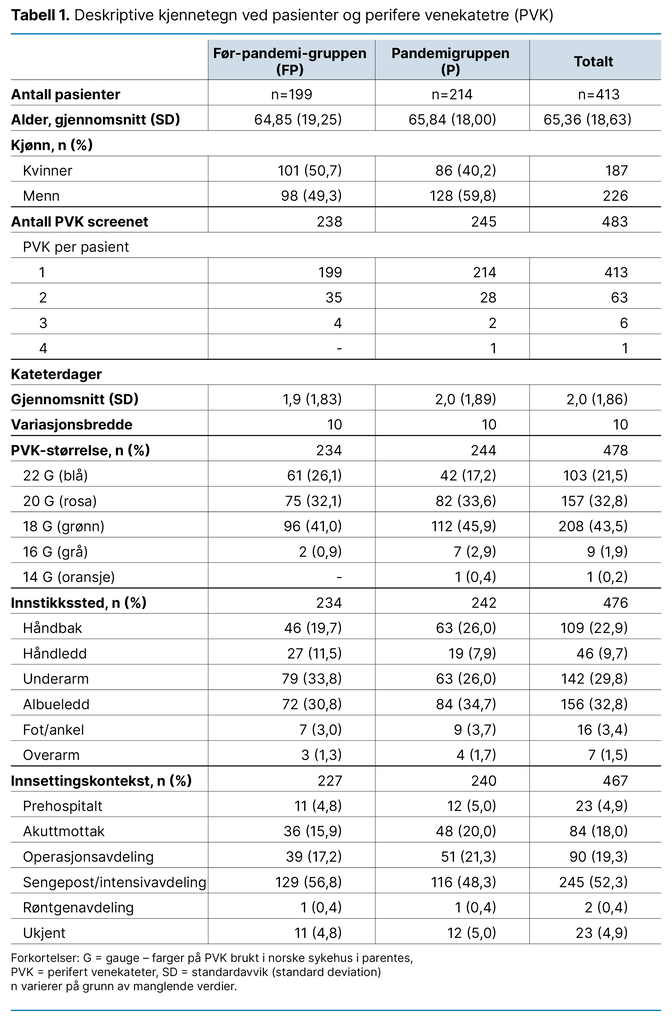
Tabell 1 viser deskriptive data for demografiske variabler og den første delen av PVK-miniQ. I FP-gruppen var 41,9 prosent av PVK-ene størrelse 18 (grønt PVK) eller større, sammenliknet med 49,2 prosent i P-gruppen. Innstikket var foretatt i ikke-anbefalte steder, som håndleddet, hos 11,5 prosent av pasientene i FP-gruppen og 7,9 prosent i P-gruppen, og i albueleddet hos 30,8 prosent i FP-gruppen, sammenliknet med 34,7 prosent i P-gruppen.
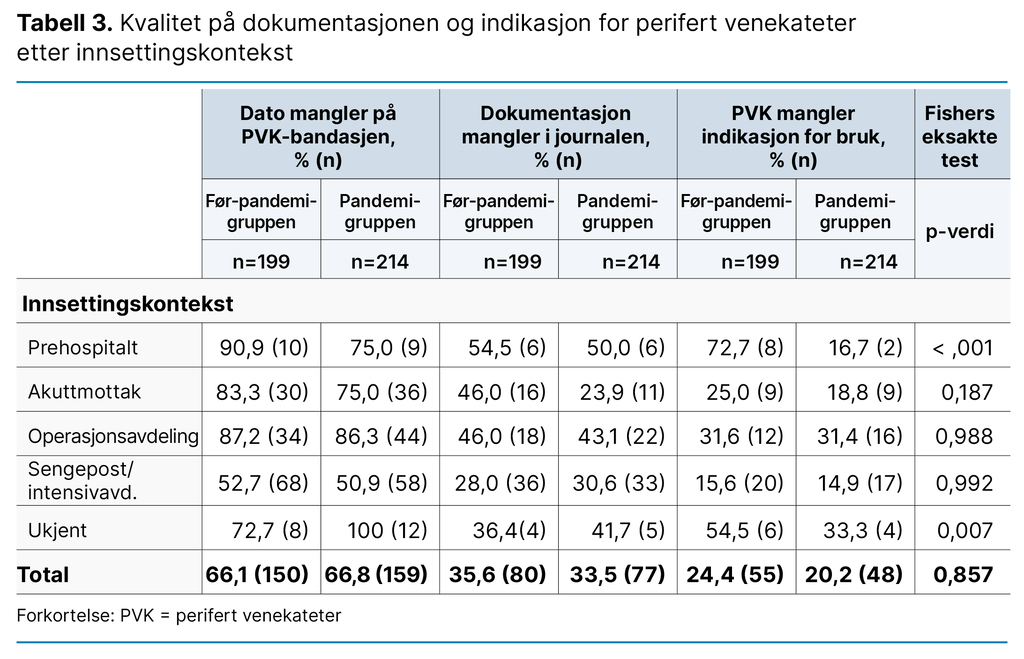
Figur 1 viser overholdelse av kunnskapsbaserte praksisanbefalinger som målt ved hjelp av PVK-miniQ i FP- og P-gruppen. Median skår var 2 i både FP-gruppen (variasjonsbredde 0–10) og i P-gruppen (variasjonsbredde 0–8), og det var ingen forskjell i skårene på PVK-miniQ mellom gruppene (p = 0,414).
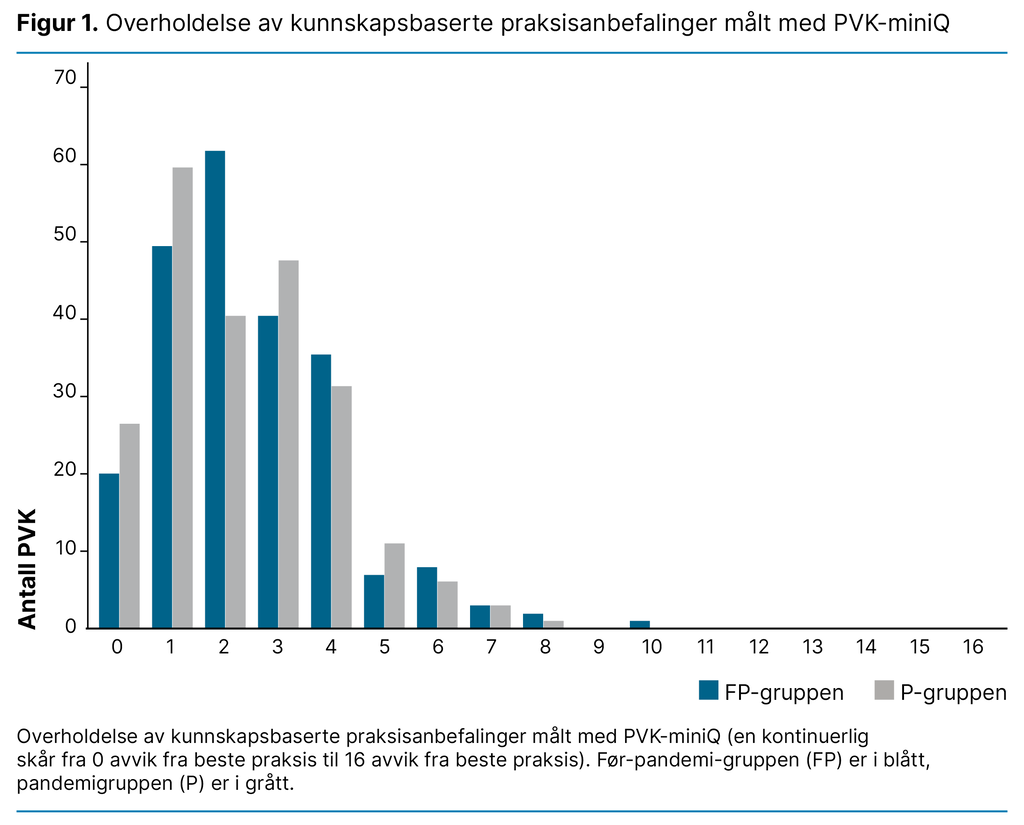
Tabell 2 viser resultatene for hver påstand i PVK-miniQ. Når det gjelder tegn på flebitt, var det hyppigste problemet smerter og rødhet i både FP-gruppen og P-gruppen. Det var en betydelig nedgang i rapportering av smerter fra FP-gruppen til P-gruppen (14,3 prosent sammenliknet med 6,7 prosent, p = 0,006). Kvinner rapporterte om smerter hyppigere både i FP-gruppen (20 prosent av kvinnene, mot 9 prosent av mennene) og i P-gruppen (11 prosent av kvinnene, mot 4 prosent av mennene, p = 0,04).
Forbedret kvalitet på stellet ble observert for påstanden «blod synlig i IV-settet», som ble funnet i 36,3 prosent av observasjonene i FP-gruppen, sammenliknet med 26,5 prosent i P-gruppen (p = 0,02). Det ble imidlertid observert dårligere kvalitet for enkelte av påstandene i PVK-miniQ i P‑gruppen: pussdannelse (0 prosent i FP-gruppen, sammenliknet med 6 prosent i P-gruppen, p = 0,001) og løsnet bandasje (15,2 prosent i FP-gruppen, sammenliknet med 24,9 prosent i P-gruppen, p = 0,008).
I FP-gruppen var det blodsøl på 77,5 prosent av alle PVK-er plassert i albueleddet, sammenliknet med 78,7 prosent i P-gruppen. Resultater for tilsølte bandasjer på PVK innlagt i underarmen var 27,0 prosent i FP-gruppen og 43,2 prosent i P-gruppen. Blant de 15 tilfellene av pussdannelse var det få pasienter som opplevde andre tegn på infeksjon; bare én opplevde smerter, tre rødhet, fire ødemer og ingen varme.
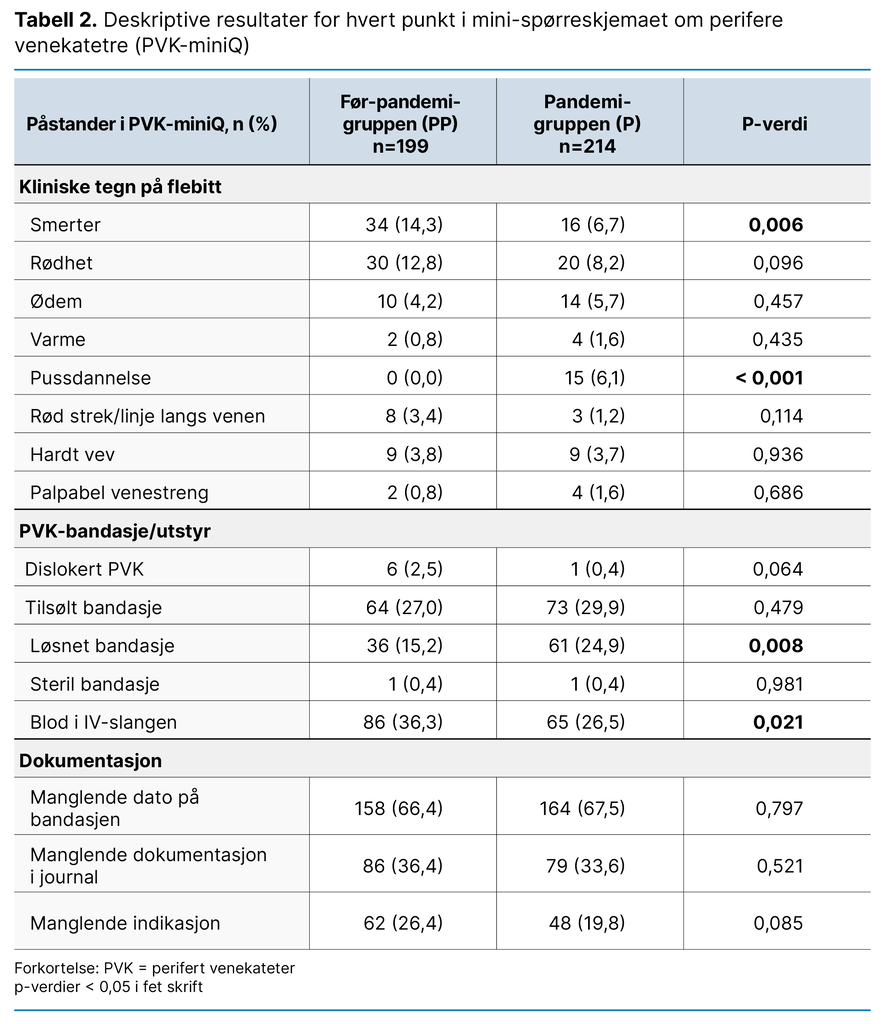
Tabell 3 viser andeler av dokumentasjon av innleggelsesdato på PVK-bandasjen eller pasientjournalen samt dokumentasjon av indikasjon for bruk i pasientjournalen i FP-gruppen versus P-gruppen. Siden det var svært få PVK-er som ble lagt inn på CT- eller MR-avdelinger (se tabell 1), ble disse avdelingene utelatt fra tabell 3.
I pandemigruppen var det en lavere andel av de PVK-ene som ble lagt inn av ambulansepersonell, som manglet dokumentasjon av innleggelsesdato på bandasjen og dokumentasjon av PVK og indikasjon i pasientjournalen, sammenliknet med FP-gruppen. De PVK-ene som hadde ukjent innleggelseskontekst, hadde imidlertid dårligere dokumentasjon i pandemiperioden sammenliknet med før pandemien. Den generelle dokumentasjonen på tvers av alle avdelinger var lik i P-gruppen og FP-gruppen.
Diskusjon
Vi observerte enkelte indikasjoner på forbedret kvalitet i pandemiperioden, som mindre smerter og færre PVK med blod i IV-settet. Vi observerte imidlertid også enkelte indikasjoner på lavere kvalitet, med flere løse bandasjer og økt forekomst av pussdannelse.
Siden PVK-miniQ viste høyere reliabilitet i den samlede skåren, konkluderer vi med at overholdelsen av de kunnskapsbaserte retningslinjene generelt var den samme under normale omstendigheter og i en situasjon der det ble pålagt retningslinjer for pandemi. I begge undersøkelsene var det vanlig med avvik fra bandasjestatus og dokumentasjon av indikasjon og innleggelse av PVK.
Håndtering og stell av PVK under covid-19-pandemien
Totalt var kvaliteten lik i FP-gruppen og P-gruppen, og det ser dermed ut til at covid-19-pandemien ikke påvirket håndteringen og stellet av PVK i vesentlig grad. Siden dette er den første studien som sammenlikner kvaliteten på PVK før og under pandemien, er den ikke direkte sammenliknbar med andre studier. Siden PVK-komplikasjoner omfatter sykehusinfeksjoner (18), kunne vi foreta en indirekte sammenlikning med en retrospektiv studie fra Australia som bare fant mindre variasjoner i sykehusinfeksjoner mellom de studerte sykehusene før og under pandemien (24).
Det kan også foretas indirekte sammenlikninger med studier som observerte en økning i blodbaneinfeksjoner under pandemien (25). Andre studier har funnet at blodbaneinfeksjoner med opprinnelse på sykehus økte betydelig i pandemiperioden, noe som understreker behovet for smittevern og forebygging (26, 27).
I denne studien hadde vi ikke tilgang til data om sykehusinfeksjoner i blodbanen, men vi fant belegg for økt pussdannelse i PVK, til tross for den økte oppmerksomheten på hygiene og smittevern under pandemien. Pussdannelse er en indikasjon på bakteriebasert flebitt, som i sin tur kan ha blitt forårsaket av en infeksjon, og er en betennelsesreaksjon som medfører smerter, rødhet, ødem og varme (26).
Andelen av både smerter og rødhet avtok fra FP-gruppen til P-gruppen, og antallet som rapporterte varme og ødem, var lite i begge gruppene. Den ulike forekomsten av pussdannelse på tvers av målingene kan skyldes utilstrekkelig opplæring i bruken av PVK-miniQ under pandemien, siden hver avdeling brukte sitt eget personale med henblikk på å forebygge spredning av covid‑19.
Siden kvinnelige pasienter tidligere har vist seg å være mer tilbøyelig enn menn til å oppleve smerter som et tegn på flebitt (6), er det viktig å bemerke at det under pandemiperioden var færre kvinner enn menn som ble innlagt på avdelingene og enhetene. Ulikheten i PVK-relaterte smerter ble imidlertid funnet både i FP-gruppen og P-gruppen, og den ulike kjønnsfordelingen mellom gruppene skal derfor ikke ha noen betydning for resultatene.
Selv om det forekom få avvik fra beste praksis for stell av PVK på tvers av målingene, var det likevel noen avvik som understreker viktigheten av løpende klinisk vurdering og kontinuerlig opplæring av helsepersonell (12). Smerte og rødhet var de mest utbredte avvikene, og forekomsten i begge undersøkelsene var stort sett sammenliknbar med andre studier. Blanco-Mavillard og medarbeidere fant at rundt 5 prosent opplevde smerter, og det ble funnet rødhet hos 6 prosent av alle pasienter med et PVK (27).
Alexandrou og medarbeidere fant at 10 prosent av alle PVK-er globalt var smertefulle (1). Høvik og medarbeidere har tidligere funnet 13 prosent smerte og 10 prosent rødhet, og en tilsvarende gjennomsnittlig skår på PVK‑miniQ på 2,04 (28). En studie fra Nepal fant imidlertid en mye høyere forekomst av smerte: hos omtrent > 40 prosent av pasienter med et PVK, og en noe høyere gjennomsnittlig skår på PVK-miniQ på 2,37 (23).
Den konsistente kvaliteten som ble observert under de to undersøkelsene i denne studien, vil delvis kunne skyldes den normale eller sågar reduserte arbeidsmengden man opplevde på tidspunktet da undersøkelsen som ble gjennomført under pandemien, ble foretatt (29). Studier fra andre land som hadde flere covid-19-pasienter enn Norge, fant at sykepleierne opplevde økt arbeidsbelastning og arbeidsrelatert stress på grunn av pandemien (20, 30, 31). Det er derfor tenkbart at kvaliteten på stellet av PVK kunne ha blitt nedsatt dersom pasienttallet hadde overskredet det normale nivået.
Styrker og svakheter
Siden denne studien ble foretatt på ett enkelt sykehus, beskriver resultatene situasjonen på et universitetssykehus i Norge der forekomsten av covid-19-pasienter var lav i måleperioden. En studieperiode med flere tilfeller av covid-19, og dermed mer arbeid for sykepleierne, kunne ha resultert i lavere kvalitet på PVK i pandemigruppen. En videre begrensning består i at vi ikke registrerte hvor mange pasienter som var utilgjengelige (under behandling) eller ikke samtykket, og heller ikke hvilket medikament som ble gitt via PVK.
Antallet deltakere i hver undersøkelse var imidlertid det samme, og det er derfor ingen grunn til å anta at én gruppe er mindre representert enn den andre. PVK-screeningen ble ikke forhåndsvarslet, og studien reflekterer derfor den faktiske kvaliteten på håndtering og stell av PVK. Det er en vesentlig styrke at alle de 14 sykehusavdelingene var involvert i begge spørreundersøkelsene.
Konklusjon
Denne studien fant at selv om det var en synkende forekomst av enkelte avvik fra retningslinjene for PVK, var det andre som økte, og samlet sett var det liten forskjell i håndtering og stell av PVK før og under den første bølgen av covid-19-pandemien. Disse funnene støtter tanken om at sykepleiere er i stand til å opprettholde et standardisert stell av PVK i utfordrende situasjoner. Pandemien økte imidlertid oppmerksomheten på smittevern generelt.
Det er likevel et paradoks at stellet av PVK ikke ble forbedret, gitt den reduserte arbeidsmengden i vår sykehuskontekst. Vår studie fremhever dermed de utfordringene som er forbundet med kunnskapsbasert stell av PVK under en pandemi. Det er behov for å etablere rutiner for opprettholdelse av kvalitet før den neste pandemien inntreffer. Disse bør inkludere både nettbasert opplæring og standarder for kvalitetsovervåkning i pandemisituasjoner.
Interessekonflikter
Lise Tuset Gustad oppgir en interessekonflikt som følge av at hun er redaktør i Sykepleien Forskning. Hun deltok derfor ikke i behandlingen av eller beslutningsprosessen vedrørende dette bidraget. For å sikre en upartisk og rettferdig gjennomgang og redaksjonell prosess ble manuskriptet behandlet av en utnevnt setteredaktør.
Åpen tilgang CC BY 4.0
Hva studien tilfører av ny kunnskap
Endret terminologi i overskriften fra "bruk" til "håndtering".
Mest lest
Doktorgrader
Selvrealisering og betydning for helsesykepleieres fortsatte yrkesutøvelse. En kvalitativ studie.
Dårlig samvittighet hos sykepleiere - En multimetodestudie om sykepleieres erfaring med dårlig samvittighet i sykehjem og hjemmebasert omsorg
Helserelatert livskvalitet og mental helse etter ekstremt prematur fødsel
Å leke med dukker i sykepleierutdanningen


















0 Kommentarer