Lindrende behandling i livets sluttfase på en intensivavdeling − et kvalitetsprosjekt
Bakgrunn: Helsedirektoratet har utgitt nasjonale faglige råd for lindrende behandling i livets sluttfase. Mange døende intensivpasienter har stor symptombyrde. For å sikre at lindrende behandling er av god kvalitet, er det nødvendig å undersøke om klinisk praksis er i tråd med gjeldende anbefalinger.
Hensikt: Å undersøke dokumentert praksis av lindrende behandling i livets sluttfase for pasienter ved en intensivavdeling. Vi ville også undersøke om praksisen var i tråd med de nasjonale faglige rådene.
Metode: Kvalitetssikringsprosjekt med retrospektiv gjennomgang av pasientjournaler. Vi utførte deskriptive, kvantitative analyser. Utvalget var voksne pasienter over 18 år som døde på en intensivavdeling ved et universitetssykehus i Norge i 2021.
Resultat: Totalt døde 88 pasienter. Av disse ble 69 pasienter inkludert. Mediantiden fra livsforlengende behandling ble avsluttet til døden inntraff, var tolv minutter. Det fantes en dokumentert tiltaksplan for å avslutte behandlingen hos 13 prosent av pasientene. Det var ikke dokumentert smerteskår hos våkne pasienter. Critical Care Pain Observation Tool (CPOT) var dokumentert brukt på 16,7 prosent av pasientene med nedsatt bevissthet, på 58,3 prosent av de komatøse pasientene, og på 44,7 prosent av de sederte pasientene. Ingen av pasientene som var våkne eller komatøse, fikk kontinuerlig infusjon av symptomlindrende legemidler, kun støtdoser. Sederte pasienter fikk infusjon med opioider og/eller sedasjon. Det var ikke dokumentert samtaler med de våkne pasientene. Pårørendesamtaler var dokumentert av 94,2 prosent av legene og 65,2 prosent av intensivsykepleierne.
Konklusjon: Studien viser at det var mangler i dokumentasjonen av smertevurdering og tiltaksplaner for døende intensivpasienter. Det var også mangler i dokumentasjonen av informasjon til pasientene.
Referer til artikkelen
Fjøsne K, Klepstad P, Gjeilo K. Lindrende behandling i livets sluttfase på en intensivavdeling − et kvalitetsprosjekt. Sykepleien Forskning. 2023; 18(92261):e-92261. DOI: 10.4220/Sykepleienf.2023.92261
Introduksjon
Målet med intensivbehandling er å opprettholde funksjonen i vitale organer hos kritisk syke pasienter. Selv om pasientene får avansert intensivmedisinsk behandling, er det mange som dør (1). I 2021 døde 10,2 prosent av pasientene på norske intensivavdelinger, og dette tallet har endret seg lite de siste fem årene (2).
Lindrende behandling til pasienter i livets sluttfase på intensivavdelinger er derfor et aktuelt kompetanseområde. For at pasientens behov for symptomlindring skal bli ivaretatt, må intensivsykepleierne ha kunnskap og kompetanse innen lindrende behandling (3).
Internasjonal litteratur viser at intensivpasienter i livets sluttfase kan ha mange ubehagelige symptomer, der smerte, angst og dyspné er vanligst (1, 4, 5). Behandlingen av symptomene er imidlertid ofte utilstrekkelig (6). Implementering av tiltaksplaner og protokoller for lindrende behandling på intensivavdelinger gir økt bruk av smertestillende og beroligende legemidler og dermed lavere symptombyrde (1, 7). Likevel er det mangel på retningslinjer og tiltaksplaner for lindrende behandling på intensivavdelinger, og det varierer stort om disse brukes i klinisk praksis (5, 8).
I Norge finnes det ikke en egen nasjonal retningslinje for lindrende behandling på intensivavdelinger. Imidlertid har Helsedirektoratet utgitt nasjonale faglige råd for lindrende behandling i livets sluttfase. De faglige rådene skal bidra til at pasientene får lindrende behandling som er faglig forsvarlig og kunnskapsbasert (9).
De nasjonale faglige rådene påpeker at ulike tiltak for å lindre eksempelvis smerte, dyspné, angst og uro alltid skal vurderes. Forslag til tiltak og mulige behov for symptomlindrende legemidler bør dokumenteres i en tiltaksplan, og det må utføres regelmessig kartlegging av pasientens symptombyrde. I tillegg må kommunikasjonen med pasientene og de pårørende ivaretas (9).
De nasjonale faglige rådene er generelle råd, og helseforetakene er ansvarlig for at rådene følges (9). Helsetjenestene har plikt til å utføre kvalitetsforbedringsarbeid. Det er nødvendig å undersøke om klinisk praksis er i tråd med gjeldende anbefalinger (10, 11).
Hensikten med denne studien var å beskrive dokumentert praksis for vurdering av smerter, legemiddelbehandling av symptomer, tiltaksplaner og kommunikasjon med pasienter i livets sluttfase og deres pårørende på intensivavdelingen. Vi ville også undersøke om praksisen er i tråd med nasjonale faglige råd for lindrende behandling i livets sluttfase. Vi tok utgangspunkt i følgende forskningsspørsmål:
«Hvordan er dagens dokumenterte praksis av lindrende behandling i livets sluttfase for pasienter på en intensivavdeling?»
Metode
Design
Studiedesignet er en retrospektiv observasjonsstudie (12) med gjennomgang av pasientjournaler i tidslinjen fra livsforlengende behandling ble avsluttet, og frem til pasienten døde. Studien var også et kvalitetssikringsprosjekt ved en intensivavdeling der formålet var å oppsummere dagens dokumenterte praksis. Resultatene skulle evaluere kvaliteten på dagens praksis (13).
Utvalg
Utvalget besto av pasienter over 18 år som døde på Hovedintensiv på universitetssykehuset St. Olavs hospital i 2021 uansett innleggelsesårsak. En tilbaketrekking av livsforlengende behandling eller bestemmelse om ikke å trappe opp behandlingsnivået skjedde før døden. Pasienter som ble organdonor, og pasienter som døde under operasjon eller på tross av aktivt forsøk på livsforlengende behandling, eksempelvis hjerte- og lungeredning ved hjertestans, ble ekskludert fra studien.
Datasamlingsmetode
Dataene ble hentet fra elektronisk anestesi- og intensivjournal og elektronisk pasientjournal. Variablene som ble brukt ved datasamlingen, er basert på Helsedirektoratets nasjonale faglige råd for lindrende behandling i livets sluttfase (9). Variablene var følgende: «alder», «kjønn», «årsak til innleggelse», «antall døgn innlagt før død», «tid fra avslutning til død», «bevissthet ved avslutning», «respirasjonsstøtte ved avslutning».
For smertevurdering undersøkte vi om det var dokumentert bruk av vurderingsverktøyene Numeric Rating Scale 0–10 (NRS) eller Critical Care Pain Observation Tool (CPOT) (14). Lokal prosedyre for smertevurdering på avdelingen tilsier at hvis pasienten responderer, brukes NRS. For pasienter som ikke kommuniserer, registreres CPOT fast én gang per vakt samt ved behov, eksempelvis ved leieendring.
Vi undersøkte hvorvidt det var dokumentert en individuell tiltaksplan. En tiltaksplan inneholder tiltak for symptomlindring og en plan for mulige behov for legemidler som kan oppstå (9).
Videre undersøkte vi hvilke symptomlindrende legemidler pasienten fikk mot smerte, surkling i luftveier, angst og uro samt medikamentdose før og etter avslutning. Avslutning er definert som når livsforlengende behandling stoppes. Infusjonshastigheten på legemidlene ble registrert 15 minutter før avslutning og rett før dokumentert dødstidspunkt.
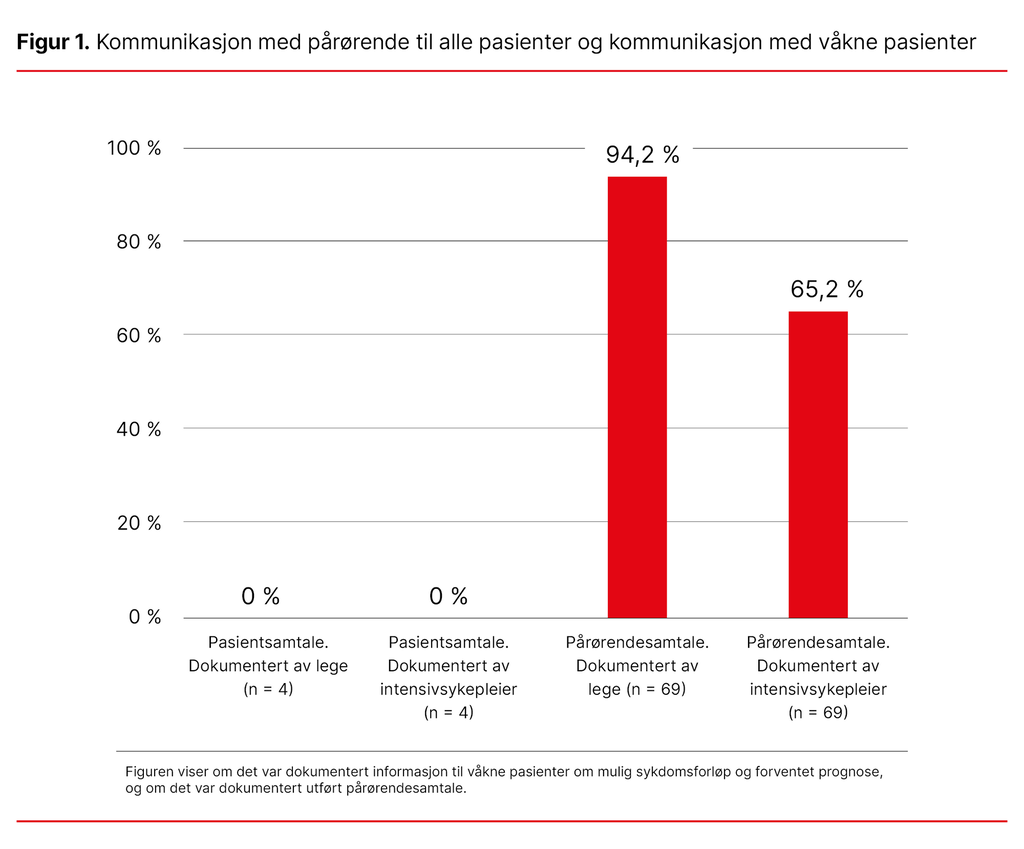
For å kartlegge kommunikasjonen undersøkte vi om hvorvidt det var dokumentert informasjon til våkne pasienter om mulig sykdomsforløp og forventet prognose. Det ble også undersøkt hvorvidt det var dokumentert pårørendesamtale av intensivsykepleier og lege, og hvorvidt pårørende var til stede ved avslutning.
Det ble ikke registrert vurderinger om angst og uro. Richmond Agitation Sedation Scale (RASS) er et verktøy for å vurdere sedasjonsdybden, der angst og uro inngår som elementer (15). På avdelingen brukes dette kun som mål på sedasjonsdybde.
Pasientene ble kategorisert i fire grupper basert på dokumentert bevissthetsnivå: 1) sederte pasienter, 2) komatøse ikke-sederte pasienter, 3) pasienter med nedsatt bevissthet, og 4) våkne pasienter.
Før datasamlingen startet, pilottestet vi skjemaet med variablene (12) på fire pasienter. Datagjennomgang ble utført februar 2022 til mars 2022 av førsteforfatteren. I tilfeller der det var tvil om kategoriseringen av dataene og om hvorvidt behandlingen fulgte retningslinjer eller ikke, ble hvert enkelt tilfelle diskutert med andreforfatteren.
Dataanalyse
Vi utførte deskriptive analyser i analyseprogrammet Statistical Package for the Social Sciences (SPSS), versjon 27 (16). Deskriptiv analyse er brukt for å beskrive og sammenfatte dataene. Kategoriske variabler fremstilles med antall (n) og prosent (%).
Kontinuerlige variabler er fremstilt med sentraltendens og spredning. Normalfordelte data er presentert med gjennomsnitt og standardavvik (SD), og ikke-normalfordelte data med median og interkvartil bredde (IQR, interquartil range) (12).
Etiske vurderinger
Dette prosjektet var en retrospektiv studie, og pasientbehandlingen ble ikke endret eller påvirket av prosjektet. Prosjektet var et internt kvalitetssikringsprosjekt som falt utenfor mandatet til Regional etisk komité for medisinsk og helsefaglig forskningsetikk (REK), og var ikke omfattet av helseforskningslovens saklige virkeområde, se §§ 2 og 4.
Prosjektet ble ledelsesforankret i ansvarlig klinikk i tråd med helsepersonellovens krav til kvalitetssikring, se § 26 (17). Prosjektlederen fylte ut et egenevalueringsskjema for Data Protection Impact Assessment (DPIA). Klinikkens forskningsutvalg vurderte og godkjente prosjektet i tråd med sykehusets prosedyre for kvalitetssikringsprosjekter og personvern. Vi fulgte sykehusets prosedyrer for sikker lagring på et dedikert filområde.
Resultater
Beskrivelse av utvalg
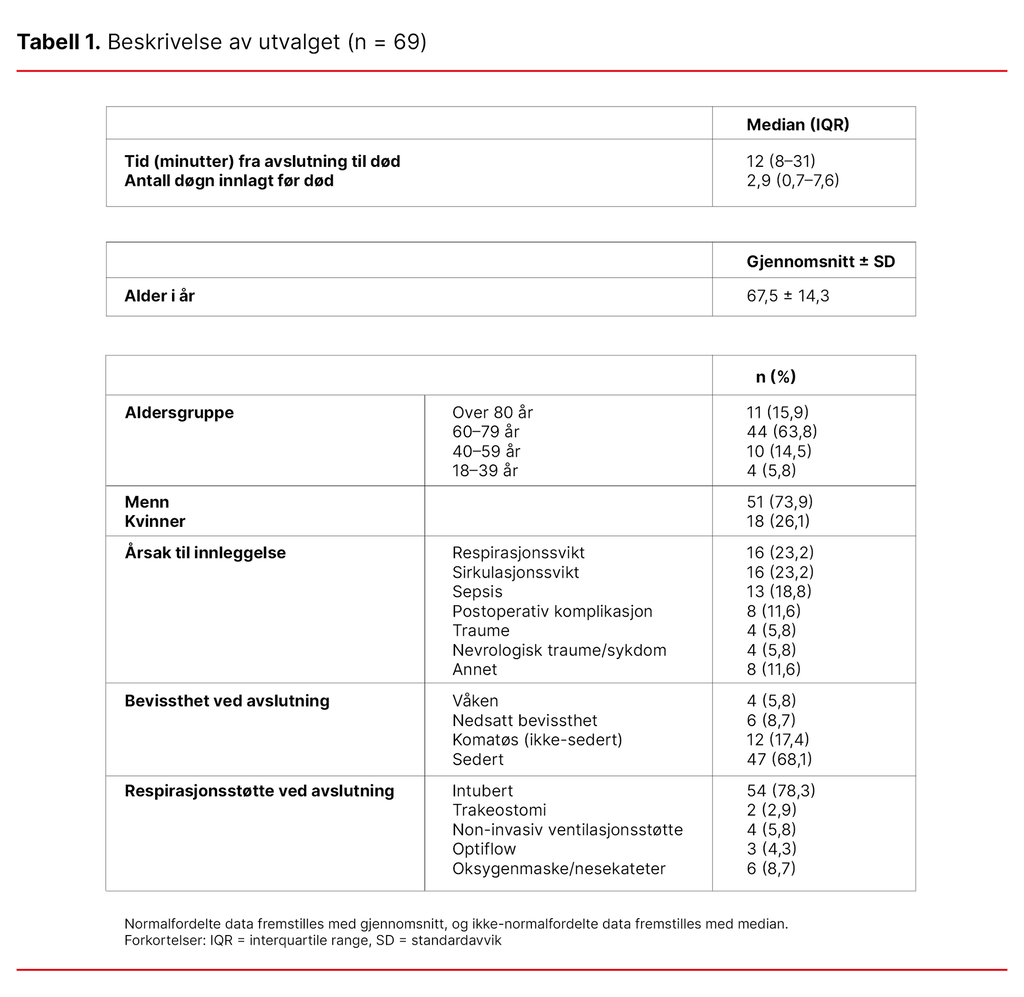
Totalt døde 88 pasienter. Av dem ekskluderte vi elleve pasienter som ble organdonorer, og åtte pasienter som døde under operasjon eller etter aktivt forsøk på livsforlengende behandling. Vi analyserte 69 pasientjournaler. Majoriteten av pasientene var menn (73,9 prosent), og de hyppigste innleggelsesårsakene var respirasjonssvikt (23,2 prosent) og sirkulasjonssvikt (23,2 prosent) (tabell 1).
Som vist i tabell 1 var mediantiden fra avslutning til død tolv minutter, og antallet døgn innlagt før død var 2,9 (median). De fleste av pasientene var over 60 år (79,7 prosent), og kun fire pasienter var under 39 år (5,8 prosent). Flertallet av pasientene var sederte (68,1 prosent).
Tiltaksplan og symptomvurdering
Det fantes en skriftlig tiltaksplan for avslutning av livsforlengende behandling hos ni (13 prosent) av pasientene (n = 69). Smerte rangert med selvrapporteringsverktøyet NRS 0–10 var ikke dokumentert hos de fire våkne pasientene.
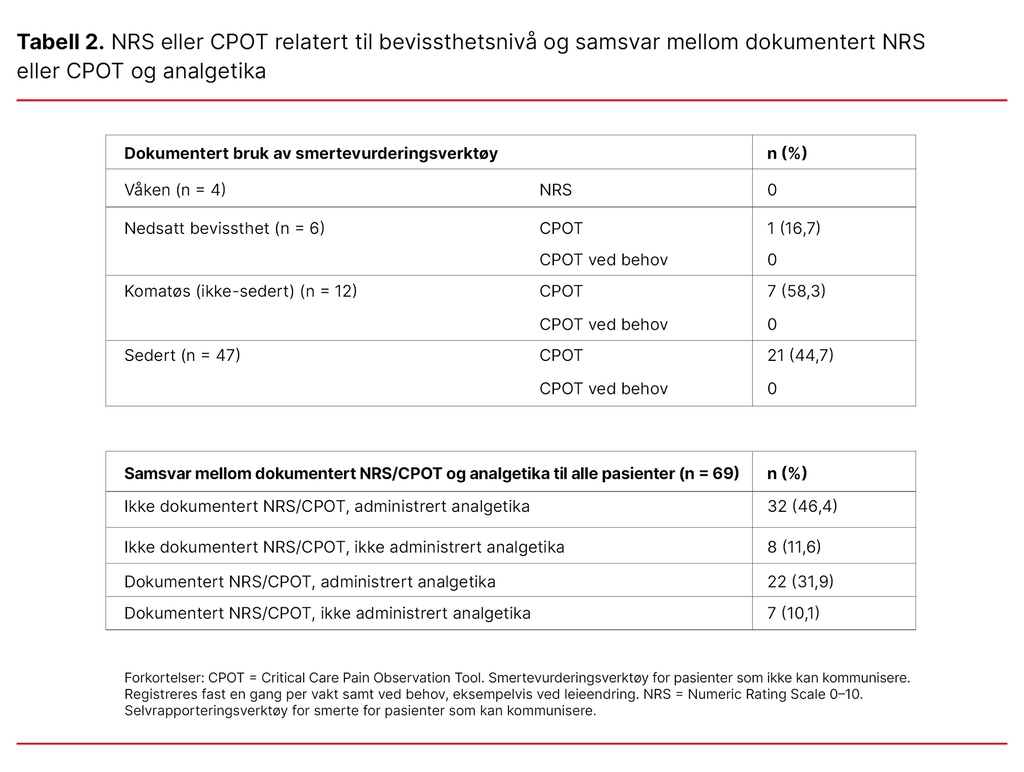
Vurdering av smerte med CPOT for pasienter med nedsatt evne til å kommunisere ble dokumentert hos 16,7 prosent av pasientene med nedsatt bevissthet, hos 58,3 prosent av de komatøse pasientene og hos 44,7 prosent av de sederte pasientene.
Det var ikke dokumentert CPOT ved behov hos noen av pasientene. Analgetika ble gitt like hyppig til pasienter uten dokumentert smertevurdering som pasienter med dokumentert smertevurdering (tabell 2).
Symptomlindrende legemidler
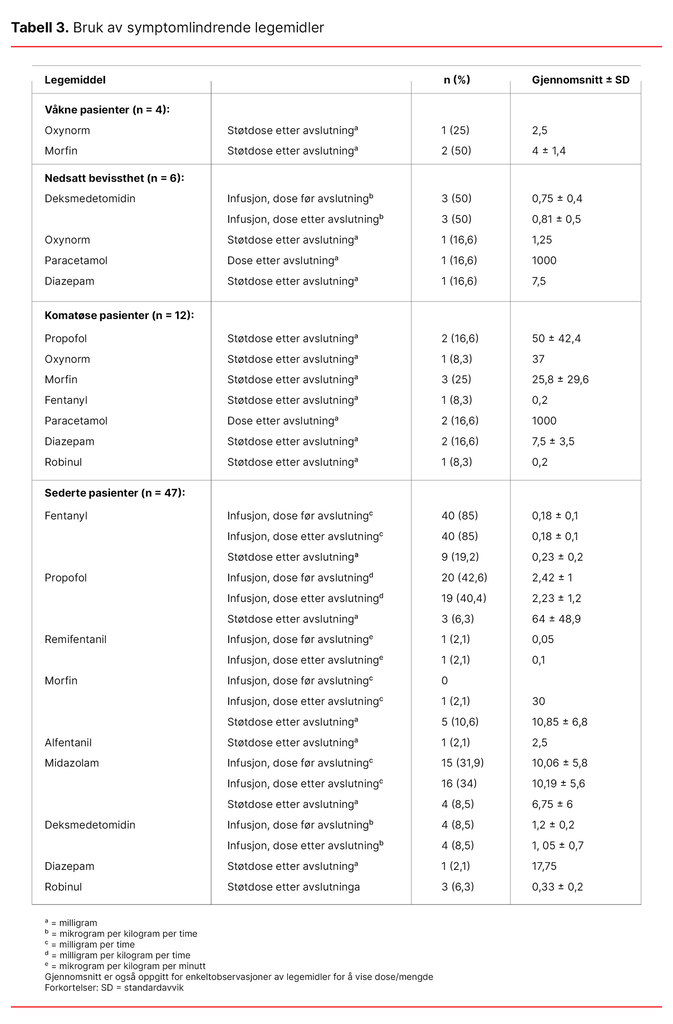
Ingen av de våkne pasientene fikk kontinuerlig infusjon av symptomlindrende legemidler, men tre av de fire våkne pasientene fikk støtdoser med opioider (tabell 3).
Som vist i tabell 3 fikk en av pasientene med nedsatt bevissthet opioider, en fikk paracetamol, og en pasient fikk diazepam etter avslutning. Ingen komatøse pasienter fikk kontinuerlig infusjon med symptomlindrende legemidler (tabell 3).
Tabell 3 viser at sederte pasienter (n = 47) fikk infusjon med opioider og/eller sedasjon. Dosen før og etter avslutning av livsforlengende behandling var tilnærmet lik, bortsett fra for en pasient som kun fikk remifentanil, og for en pasient som fikk infusjon av morfin i tillegg til annen analgetika. Om lag en firedel og en tidel av de sederte pasientene fikk støtdose med henholdsvis analgetika og sedativer etter at livsforlengende behandling var avsluttet.
Kommunikasjon med pårørende og pasienter
Det var ingen dokumenterte samtaler med de våkne pasientene, verken av sykepleier eller lege. For alle pasientene var samtaler med pårørende dokumentert av legen hos 94,2 prosent og av intensivsykepleieren hos 65,2 prosent (figur 1). Majoriteten av pasientene hadde pårørende til stede ved avslutning (74 prosent).
Diskusjon
Studien viste at det var mangel på dokumentert smertevurdering og tiltaksplan. For våkne intensivpasienter var det dessuten mangel på dokumentert informasjon da livsforlengende behandling ble avsluttet.
Vurdering av smerte
I denne studien var det ikke dokumentert smertevurdering for noen av de våkne pasientene og om lag halvparten av de ikke-våkne pasientene. I de nasjonale faglige rådene (9) anbefales regelmessig observasjon av pasientens kliniske tilstand for å oppnå god symptomlindring.
Avdelingens lokale retningslinje for smertevurdering sier dessuten at pasienter skal vurderes med NRS eller CPOT én gang per vakt samt ved behov. Resultatene samsvarer med funn fra andre studier (18, 19), som viser at det er lav prosentandel av intensivpasientene med dokumentert smertevurdering.
Funnene er overraskende siden det er en forutsetning for god behandlingen av plagsomme symptomer hos døende pasienter at det er utført systematisk symptomvurdering med validerte verktøy, både hos våkne og sederte pasienter (14, 20). Denne studien undersøkte ikke hvorfor smertevurdering var dårlig dokumentert. En mulig årsak kan være at intensivsykepleieren har spurt pasienten uten å dokumentere svaret, eller at intensivsykepleieren oppfattet pasienten som så sedert eller komatøs at vedkommende mente at det var overflødig å vurdere med CPOT.
Resultatene viser imidlertid at det ble administrert analgetika like hyppig til pasientene der det ikke var dokumentert smertevurdering, som ved dokumentert smertevurdering. Uansett bør intensivsykepleierne dokumentere vurderingene de gjør (17), og man kan ikke utelukke at pasienter har hatt smerte som har blitt oversett på grunn av mangel på systematisk kartlegging og dokumentasjon.
Tiltaksplan
I studien vår hadde kun 13 prosent av pasientene en dokumentert tiltaksplan. Det er beskrevet i de nasjonale faglige rådene at en plan for å avslutte livsforlengende behandling samt mulige behov for legemidler bør dokumenteres i pasientjournalen (9). Tidligere studier (21, 22) har vist at intensivsykepleiere ønsker en skriftlig tiltaksplan for å kunne gi best mulig omsorg til pasienter i livets sluttfase.
En studie (23) fant at sykepleiere vurderte tiltaksplan som et nyttig verktøy. En annen studie (24) fant at mangel på klare retningslinjer ved avslutning av livsforlengende behandling gjorde at intensivsykepleierne ble usikre på hva som var riktig tiltak når den livsforlengende behandlingen ble avsluttet. Et mulig problem med å bruke tiltaksplaner var at standardiserte tiltaksplaner hindret behandling tilpasset hver enkelt pasient (25, 26).
En mulig forklaring på hvorfor kun ni av pasientene hadde en dokumentert tiltaksplan, er at intensivsykepleierne kan varsle legen når symptomer oppstår, og tiltak og medikamenter kan da forordnes fortløpende. Dette er mulig i en enhet med døgnkontinuerlig tilstedeværelse av lege. Det er også sannsynlig at legen og intensivsykepleieren i mange tilfeller drøftet en plan uten at dette ble nedskrevet i journalen. I tillegg kan det diskuteres om en tiltaksplan er nødvendig når mediantiden fra avslutning til død er tolv minutter.
En nederlandsk observasjonsstudie (27), der mediantiden fra avslutning til død var 20 minutter, konkluderte imidlertid med at en ny retningslinje med råd om forebygging av plagsomme symptomer var effektiv, og de fleste av pasientene viste lav symptombyrde. Dersom dette er tilfellet, vil tiltaksplaner være hensiktsmessig selv om det er kort tid fra avslutning til død.
Legemiddelbehandling av plagsomme symptomer
Resultatene i studien vår viste ingen doseøkning av legemidler før og etter avslutning hos sederte pasienter, bortsett fra hos to pasienter som fikk lagt til henholdsvis morfin eller remifentanil. Dette funnet skiller seg fra flere studier som har observert at opioiddosen ble økt når livsforlengende behandling til intensivpasienter ble avsluttet (27−29).
Denne forskjellen kan ha flere mulige forklaringer. En retningslinje eller individuell behandlingsplan for å avslutte livsforlengende behandling kan gjøre det enklere for intensivsykepleierne å øke doser av analgetika og sedativer. Dette passer med funn i den nederlandske observasjonsstudien (27), som fant at da en ny retningslinje om palliasjon ble innført, økte bruken av midazolam, propofol og opioider betydelig.
Videre kan pasientene i vår studie i utgangspunktet ha vært tyngre sedert enn i andre studier, slik at det derfor ikke var behov for å øke medikamentdosene. Vi samlet ikke inn data om sedasjonsdybde, slik at vi ikke kan sammenlikne graden av sedasjon i forløpet. I tillegg var mediantiden fra avslutning til død tolv minutter i vår studie.
I et så kort tidsintervall vil man erfaringsmessig ofte velge å gi støtdoser ved behov, noe som ble administrert til en andel av pasientene i studien vår. Når mediantiden kun er tolv minutter, kan det indikere at pasientene er så syke at de allerede er langt uti dødsfasen når behandlingen avsluttes, og derfor ikke har økt behov for lindrende legemidler. Men i studiene fra Nederland (27) og USA (28), der mediantidsintervallet fra avslutning til død var på henholdsvis 20 minutter og 42 minutter, ble legemiddeldosene økt betraktelig.
Under halvparten av de komatøse pasientene fikk analgetika, og en seksdel fikk legemidler mot angst og uro. Dette funnet samsvarer med studien fra USA (28), som viste at komatøse pasienter fikk mindre morfin enn andre pasienter. Det kan skyldes at det ikke administreres analgetika til komatøse pasienter som ikke reagerer på smertestimuli, fordi man antar at de ikke opplever smerte.
Smerte er en subjektiv opplevelse (30), og uten reaksjon på smertestimuli vil pasienten mest sannsynlig ikke ha et stort behov for analgetika. Det er derfor ikke overraskende at komatøse pasienter får lavere doser enn andre pasienter. For kritisk syke nevrointensivpasienter med minimalt bevisst tilstand, som kan oppleve smerte de ikke evner å kommunisere, er det derimot viktig at intensivsykepleierne observerer tegn på ubehag og administrerer tilstrekkelig analgetika (30, 31).
Et interessant funn var at pasientene med bevissthetsnivå «nedsatt bevissthet» og «våken» kun fikk støtdoser med symptomlindrende legemidler, og det ble gitt lave doser. Kun én pasient fikk ikke-opioide analgetika. Det blir derfor vanskelig å sammenlikne med andre studier der pasientene fikk kontinuerlig legemiddelinfusjon (27, 28).
Det kan antas at ved akutt forverring hos pasientene som var våkne, var det mer praktisk å gi analgetika ved behov. I tillegg var det manglende dokumentert smertevurdering med NRS og CPOT, noe som gjør det vanskelig å vite den reelle symptombyrden og behovet for lindrende legemidler. Erfaringsmessig kan noen intensivsykepleiere og leger være tilbakeholdne med å gi opioider til døende pasienter av frykt for bivirkninger som respirasjonsdepresjon og hypotensjon. Denne praksisen er lite kunnskapsbasert siden flere studier viser at økt bruk av opioider kan forlenge tiden fra avslutning til død (27−29).
Kommunikasjon med pasient og pårørende
Hele 94,2 prosent av de pårørende hadde hatt samtale med lege, noe som er et høyt antall sammenliknet med en studie fra USA (32), som fant at tverrfaglige møter med familien var dokumentert hos mindre enn 20 prosent av pasientene. Samtaler med pårørende er viktig ettersom det er kort vei mellom kritisk sykdom og død på en intensivavdeling.
En studie (33) viste at ærlig og klar kommunikasjon var en faktor som påvirket de pårørendes tilfredshet da pasienten var i livets sluttfase, og det forhindret posttraumatisk stress blant de pårørende. I de nasjonale faglige rådene (9) er det beskrevet at helsepersonell skal ivareta pasientens og pårørendes behov for samtale og informasjon i livets sluttfase, men vår studie undersøkte kun om det var dokumentert samtaler. Vi undersøkte ikke innholdet i informasjonen som ble gitt, eller om pårørende opplevde å få tilstrekkelig informasjon.
Det var ikke dokumentert pasientsamtale hvor det ble informert om mulig sykdomsforløp og forventet prognose, for de fire våkne pasientene, verken av intensivsykepleier eller lege. Dette er et interessant funn fordi pasientene har rett på informasjon om sin helsetilstand (34).
Studien vår undersøkte kun den dokumenterte praksisen. Forhåpentligvis har samtaler med pasienten blitt utført uten at det ble dokumentert i pasientjournalen. Likevel er det uheldig at det ikke er dokumentert hvilken informasjon pasienten fikk, eller om situasjonen var slik at det ikke var mulig å gi informasjon.
Pasienten må få fortløpende informasjon om sin tilstand, og om mulig få medvirke i beslutningsprosesser ved avslutning av livsforlengende behandling (9). Hvis ikke kan konsekvensen være at man ikke får avklart pasientens ønsker, som for eksempel behov for religiøse ritualer eller tanker om hvordan avslutningen skal foregå, eller at pasienten ikke blir trygg på at smerten og ubehaget skal lindres.
I vår studie var det kun fire pasienter som var kategorisert som våkne, slik at vi ikke kan konkludere sikkert. Funnet peker likevel på at praksisen med å gi informasjon til våkne pasienter som er kritisk syke på en intensivavdeling, må undersøkes ytterligere.
Studiens styrker og svakheter
En svakhet ved studien er at den var retrospektiv og kun kartla dokumentert praksis, noe som betyr at det kan være utført vurderinger og behandling som ikke var dokumentert. En annen svakhet var at pasientene som ikke døde på avdelingen etter at behandling var avsluttet, men som ble flyttet til sengepost, ikke ble inkludert. Informasjon om hvilken lindrende behandling de fikk før de ble flyttet, ville vært relevant for studien.
En svakhet er også at utvalget kun var fra én intensivavdeling, noe som begrenser generaliseringen. Resultatene representerer nødvendigvis ikke andre intensivavdelinger, som kan ha egne interne retningslinjer og rutiner.
En vesentlig styrke ved det retrospektive designet er at vi unngikk skjevhet (bias) ved at ingen av intensivsykepleierne eller legene på avdelingen var kjent med at dataene skulle benyttes til dette formålet. Dermed kunne de ikke påvirke resultatene (12).
Konklusjon
Studien viser mangler i dokumentasjonen av smertevurdering, tiltaksplaner og informasjon til døende intensivpasienter dersom dokumentert praksis skal være i tråd med nasjonale faglige råd for lindrende behandling i livets sluttfase.
Et særlig viktig funn var at det ikke var dokumentert informasjon til noen av de våkne pasientene. Funnene i studien understreker at det er viktig å være oppmerksom på lindrende behandling til intensivpasienter, slik at man sikrer gode rutiner for å vurdere smerte og planlegge symptombehandling i livets sluttfase.
Forfatterne oppgir ingen interessekonflikter.
Åpen tilgang CC BY 4.0.
Hva studien tilfører av ny kunnskap
Rettelse i tabell 3: Siste linje om Robinul hadde falt ut og ble derfor lagt inn 30.06.2023.
Mest lest
Doktorgrader
Selvrealisering og betydning for helsesykepleieres fortsatte yrkesutøvelse. En kvalitativ studie.
Dårlig samvittighet hos sykepleiere - En multimetodestudie om sykepleieres erfaring med dårlig samvittighet i sykehjem og hjemmebasert omsorg
Helserelatert livskvalitet og mental helse etter ekstremt prematur fødsel
Å leke med dukker i sykepleierutdanningen





















0 Kommentarer